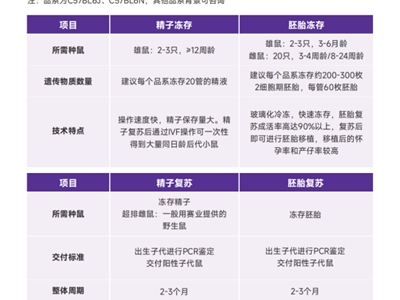
小型猪冠脉模型的影像学评价
小型猪冠脉模型中影像学评价最为直观和方便,可观察到整个支架血管段的内膜增殖、血栓、贴壁等信息,并且可以重复进行。小型猪冠脉模型中常用的影像学评价手段主要包括定量冠脉造影狭窄分析(quantitative coronary angiography, QCA)、血管内超声(intravascular ultrasound, IVUS)以及光学相干断层成像(optical coherence tomography, OCT)。由于其自身的特点不同,因此在小型猪冠脉模型的研究中所起到的作用也不尽相同,以下对此三种影像学评价方法进行分别介绍。
1.定量冠脉造影狭窄分析 QCA分析是建立在冠脉造影基础上的,因此良好的冠脉造影图像是QCA分析的基础。而QCA的基本方法即是挑选一帧适宜的冠脉造影影像,首先对其进行校准,然后通过选择近远端有软件进行分析,从而得出相应数据以进行分析。
QCA分析应由2名有经验的QCA技师分别独立地盲法分析,将全部原始数据提交数据统计中心。而分析软件多应用QUANTCOR.QCA(CAAS Ⅱ)v.5.0(Pie Medical Imaging, The Netherlands)软件包。
(1)影像的选择:在QCA分析前应首先选择好适宜分析的体位和单帧图像。由于与人冠脉造影不同,小型猪冠脉模型中造影体位有限,因此无需在许多体位中寻找,仍应遵需充分伸展和暴露支架血管段的原则。但应注意初次置入以及造影随访时的体位务必一致,以保证分析时的误差减至最小。选择单帧图像时应寻找造影剂充分充盈时的图像,并且保证图像位于心脏的舒张期。
(2)导管校准:在正式测量支架段血管时,应先校准导管。校准工作非常重要,是保证 QCA数据准确的基础。在校准时应让导管中充分充盈造影剂,并且图像清晰以及导管的轮廓清楚。校准方法可采用两点间距离法以及导管直径法等。
(3)测量:在选择好单帧造影图像以及校准导管后,测量本身显得并不复杂。选择支架段两端的两点后,软件可自动进行探测血管轮廓,从而得出相应数据。
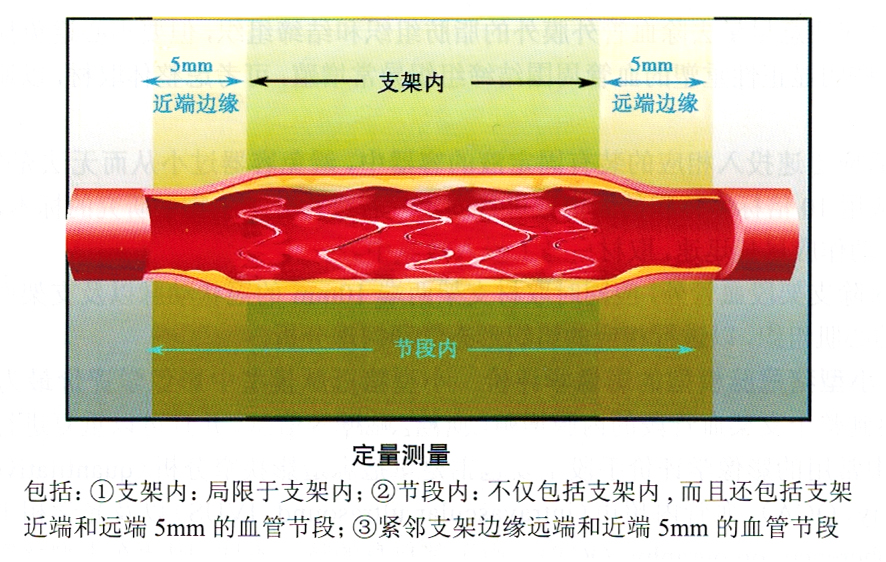
注意测量时不应只测量支架段血管,定量测量应包括:①支架内:局限于支架内;②节段内:不仅包括支架内,而且还包括支架近端和远端5mm的血管节段;③紧邻支架边缘远端和近端5mm的血管节段(图5-10)。
1)置入时观察指标:参考血管直径、球囊扩张直径、扩张比、置入后最小管腔面积。
2)复查时观察指标:参考血管直径、置入后最小管腔直径、管腔丢失、狭窄百分比。
其中需要说明的是:参考血管直径=(近端参考血管直径+远端参考血管直径)/2;球囊扩张直径=球囊膨胀最大压力时的最大直径;扩张比=球囊扩张直径/基线血管直径;管腔丢失=置入后即刻最小管腔直径一复查时最小管腔直径;狭窄百分比=(1-最小管腔直径/参考血管直径)×100%。
(4)定量冠脉造影分析变异性的影响因素
1)生物学变异性:血管紧张度导致远端血管收缩和痉挛,都会在配对测量中极大地影响到动脉直径。可通过冠脉内推注硝酸甘油(50~200μg)的方式而达到一过性的最大冠脉舒张。
2)采集变异性:包括心脏和呼吸的运动伪影、血管透视缩短、冠脉充盈不充分、造影剂过度充盈未能将重叠的血管分支与狭窄处进行分离、平面外放大和枕形失真、数字成像和储存引起的图像压缩等等。
3)测量的变异性:包括体位的选择、帧的选择、观察者间的差异以及不同的自动QCA系统之间的差异。因此如前所述要求置入和复查时体位一致、选择充分暴露血管并清晰的单帧影像、需要两名具有丰富经验的QCA分析人员,同时尽量使用同一种QCA分析软件。
2.血管内超声 由于QCA分析为二维平面的分析,受到体位、造影剂充盈和操作等诸多影响,因此存在其无法避免的缺陷。而血管内超声的检查的出现,在很大程度上解决了这一问题。IVUS可以从血管腔内观察血管壁的情况,能够完整显示血管壁横断面上管腔、管壁以及病变的全部信息,能够准确清晰的测量血管腔环绕面积、外弹力板环绕面积,从而计算出斑块或新生内膜环绕面积。并且通过其三维重建技术,可以得出斑块或新生内膜体积,从而更加准确的得到斑块或新生内膜容量负荷的信息。目前常用为Boston公司以及 Volcano公司生产的血管内超声系统,北京大学第一医院应用的血管内超声系统为前者。
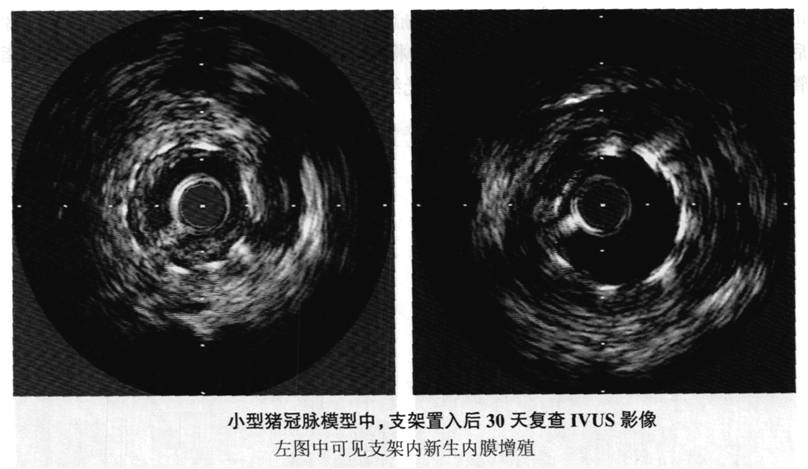
具体操作:沿0.014英寸指引导丝将IVUS导管送至支架远端,超声探头位于支架远端5mm左右,采用自动回撤装置回撤超声导管,回撤速度0.5mm/s,回撤至支架近端5mm处或血管开口处停止记录。应用图像后处理软件进行IVUS后处理分析。确定管腔环绕面积、支架环绕面积、外弹力板环绕面积,每间隔0.5~1mm测量一次,由软件计算出新生内膜面积、新生内膜体积(图5-11)。
1)主要观察指标:①参考血管面积=(近段参考血管面积+远段参考血管面积)/2;②管腔面积;③外弹力板环绕面积/支架环绕面积;④新生内膜面积=外弹力板环绕面积-管腔面积;⑤新生内膜体积;⑥最大新生内膜厚度。
2)注意事项:①建议在置入支架前先进行IVUS检查,以帮助判断血管直径,置入适合直径的支架。支架/血管为1.1/1最为适宜。②建议在置入支架后即刻复查IVUS检查,以确定贴壁良好以及获得准确扩张比。③行IVUS检查前,建议在指引导管到位后冠脉内注射硝酸甘油200μg,以避免痉挛因素影响。④必须应用自动回撤系统,固定回撤速度,否则无法应用软件进行体积分析。⑤建议在IVUS后处理分析中,每间隔5mm测量一次。
3.光学相干断层成像 光学相干断层成像系统是近十年迅速发展起来的一种新的高分辨率实时成像技术,它将光学技术与超灵敏探测器合为一体,利用弱相干光干涉仪的基本原理,检测生物组织不同深度层面对入射弱相干光的背向反射或几次散射信号,通过扫描,可得到生物组织二维或三维结构图像。它在冠心病早期诊断,指导介入治疗的实施和评价治疗效果等方面具有重要的应用价值。目前使用的血管内OCT成像仪为美国Light Lab公司生产的OCT(M2 OCT系统)。由于OCT的近红外线不能透过血液,所以必须在阻断血流的情况下才能获得理想的图像。下面就冠状动脉内OCT成像的基本方法及影响成像结果的因素简单介绍。
(1)OCT的基本操作方法
1)OCT成像仪:开机后,将OCT成像导丝与主机PIU相连接,通过Z offset键进行聚焦。然后设定导丝回撤速度,通常选择3.0mm/s,这样既可以获取满意的图像质量又可以确保50mm的扫描长度在30秒内完成,避免了长时间堵塞血管出现恶性事件。
2)高压注射器:将装有生理盐水或林格液的高压注射器与通过延长管及Y接头与OCT阻断球囊导管相连接。需要强调一点,无论使用何种冲洗液都必须肝素化。高压注射器流速的选择,我们不必拘泥于0.5ml/s或1ml/s,而是应根据扫描血管的管径大小灵活调整。
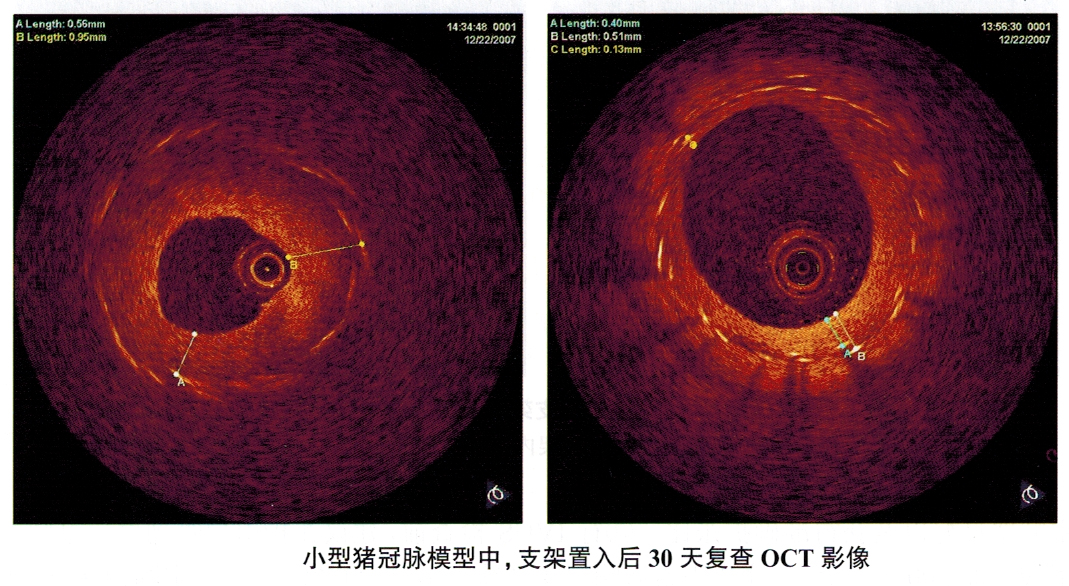
3)检查方法:①按照介入治疗常规置入指引导管就位于左或右冠状动脉口,将PCI导丝送入靶血管,通过支架段至远端固定。②将OCT阻断球囊导管沿PCI导丝送入指引导管内,直至支架段远端。③从OCT阻断球囊导管中撤出PCI导丝。④将OCT成像导丝送入OCT阻断球囊导管内,在X线透视下将成像导丝送至支架段的远端(OCT成像导丝前端的镜头位于靶病变稍远端)。⑤回撤OCT阻断球囊导管,使球囊标记点位于支架段的近端,病变段充分暴露在成像导丝下(阻断球囊与成像导丝表现为相对运动)。⑥设定好流速及压力,打开高压注射器开关,开始冲洗血管管腔。同时充盈OCT阻断球囊堵塞血管,压力可选择0.5~1.0atm。⑦OCT图像显示清晰时,开始回撤成像导丝,扫描成像。⑧成像结束后,迅速负压回吸阻断球囊,停止冲洗。⑨将OCT阻断球囊导管和成像导丝回撤至指引导管内。注意动作要轻柔,防止成像导丝内光纤折断(图5-12)。
(2)影响成像结果的因素
1)分支血管过多过大:由于OCT成像必须在阻断血流不断冲洗的情况下实现,当分支血管过多时,很难将扫描段的红细胞冲洗干净,特别是分支较大时影响成像部位的血液阻断,这时由于红细胞的影响使得成像效果欠佳。
2)血管管腔过大:冠状动脉从开口发出后,由近至远逐渐变细。一般情况下,冠状动脉近端最大管腔直径约为4~5mm。OCT阻断球囊充盈后最大直径为4.0mm,所以大多数情况下时可以充分阻断血流。但当冠状动脉血管直径超过4mm时,OCT阻断球囊就不能完全阻断血流,造成OCT图像不清楚或OCT检查失败。
3)血管过度弯曲:OCT成像导丝主要是由光导纤维构成,相对较硬易碎,柔韧性和可操作性无法和PCI导丝相比。有的冠状动脉血管曲度过大,这样OCT成像导丝无法就位,导致检查失败。
4)心脏周期运动对图像的影响:心脏节律性收缩和舒张时,会影响冠状动脉的三维形态。特别是心率较快时,成像导丝会随着心跳出现“抖动”,导致图像出现运动伪影;同时心脏收缩和舒张不同时相测量目标血管的测值也会有偏差。
5)心肌对缺血的耐受性:OCT成像时,需要对冠状动脉内的血流进行阻断,这样就会引起检查的靶血管所供应的心肌发生一过性缺血。心肌对缺血具有高度易感性,不同动物的心肌对缺血的耐受性也不一样。有的在球囊阻断时动物即会出现血压下降,心律失常等,从而要求冠状动脉内OCT成像时间尽可能缩短,甚至需要终止检查。由于第一代OCT需要阻断血流,因此对于左主干或者开口部位的支架置入,由于无法阻断血流,因而无法进行检查。
(3)OCT在小型猪冠脉模型中的作用:首先,对于IVUS可以测量的参数,诸如新生内膜面积、新生内膜厚度、管腔面积、支架环绕面积等均可以进行测量,同时由于OCT本身较高的分辨率,在动物实验研究乃至临床实践中,具有其特殊的作用。
1)OCT检测血栓:冠状动脉内易损斑块在一定的内体因素刺激下发生斑块破裂、激发血栓形成,从而成为心脏不良事件的启动子。因而除了要明确OCT在诊断易损斑块的应用价值,还应对继发血栓进行相关研究。易损斑块的不稳定性增加血管内粥样斑块的破裂进而导致局部血栓形成的风险。OCT组织分辨率高的特点同样对斑块破裂继发的血栓形成能够准确识别。对于小型猪动物实验中,在体观察有无支架内血栓形成,相比IVUS来说, OCT具有相当明显的优势。
2)OCT评估支架情况:IVUS对冠状动脉介入治疗支架内血管情况的检测一直作为诊断标准,但由于IVUS分辨率较低,而支架本身的特性干扰了IVUS对放置支架后出现的血栓、支架内再狭窄等难于提供更详细的信息。近几年,随着OCT已经在临床上逐渐普及,用OCT评价支架置入后急性期支架的贴壁程度,以明确支架对血管壁的作用机制、支架内血栓形成等情况,判断围术期血管的损伤。支架置入后数月到数年,用OCT评价支架置入后,近远期的效果。OCT可以探测支架支撑杆表面覆盖组织的厚度、面积、分布和血栓形成,以判断支架内内膜组织的覆盖程度。在临床实践中人们发现,药物洗脱支架在减少支架内血管再狭窄发生率的同时也抑制了支架表面血管内膜的再修复,从而在支架处为晚期血栓形成提供了适宜环境。因此,在为冠心病患者治疗的同时,需要对支架本身所带来的潜在危险进行评估。因此,可以用OCT评价未被覆盖的支架支撑杆的情况,决定是否采取更长时间的抗血小板治疗。此外,OCT也可用于评价重叠的药物洗脱支架贴壁不良情况,甚至于通过OCT下内膜和支架间的距离可以帮助判断是否内皮化。