罗凌飞团队通过构建早衰斑马鱼模型发现抗癌药物sapanisertib的抗衰老潜力和作用机制
随着人口老龄化加剧,如何延缓衰老、实现健康老龄化,已成为生物医学领域关心的热点和亟待解决的难题。为了应对这一挑战,科学家们一直在寻找能够有效延缓衰老的药物。传统的用于抗衰老研究的衰老动物模型各有局限:小鼠等哺乳动物模型实验周期长,严重限制了高通量药物筛选的效率;而果蝇等无脊椎动物模型在器官结构和生理功能上与人类存在较大差异,难以反映人类衰老的复杂过程。因此,开发一种能够模拟人类衰老过程、同时适用于高通量筛选的脊椎动物模型,对于发现潜在的抗衰老药物至关重要。
近日,复旦大学生命科学学院罗凌飞团队在PNAS上发表了题为"Establishment and application of a zebrafish model of Werner Syndrome identifies sapanisertib as a potential antiaging drug"的研究论文。该研究成功构建了一种衰老斑马鱼动物模型作为高效的抗衰药物筛选平台,并从小规模筛选中发现抗癌药物sapanisertib具有延缓衰老的潜力。

Werner综合征是一种罕见的遗传性早衰疾病,由WRN基因突变引起,患者表现出基因组不稳定、细胞衰老和寿命缩短等衰老特征,这些特点使其成为研究人类自然衰老的“黄金模型”[1, 2]。然而,Wrn基因敲除小鼠未能再现人类Werner综合征表型,制约了相关药物的研发[3, 4]。研究人员在斑马鱼ENU正向遗传诱变筛选中,发现了一个名为meteor的斑马鱼突变体,该突变体wrn基因发生突变,使得斑马鱼在幼鱼期就表现出与Werner综合征患者相似的早衰特征。作为早衰斑马鱼模型,此突变体因幼鱼个体小与实验周期短以及作为脊椎动物与人类较高的基因同源程度等特征,成为理想的高通量抗衰药物筛选平台(图1)。
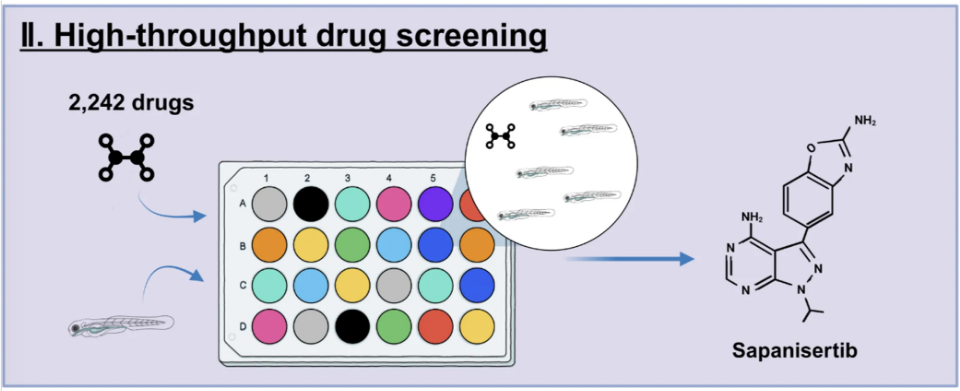
图1 利用斑马鱼早衰模型进行高通量抗衰老药物筛选。
借助这一高效筛选模型,研究人员在首轮小规模筛选中从2242个已批准药物中筛选出了抗癌药物sapanisertib作为潜在抗衰老药物。sapanisertib是一种口服抗癌药物,目前处于临床试验阶段,主要用于治疗乳腺癌、子宫内膜癌和肾细胞癌等晚期实体瘤。实验结果显示,sapanisertib显著改善了多种早衰表型,包括降低细胞衰老标志物SA-β-Gal活性、减少DNA损伤以及延长突变体寿命等。机制研究表明,sapanisertib主要通过同时抑制mTORC1和mTORC2通路发挥作用。此外,sapanisertib不仅在早衰斑马鱼中显示出抗衰老作用,在自然衰老的斑马鱼以及人类成纤维细胞中同样展现出延缓衰老、延长细胞寿命等效果,预示着该药物在治疗Werner综合征、改善衰老表型进而延缓衰老方面具有潜在的重要应用价值。
综上所述,该研究通过建立Werner综合征的斑马鱼模型,成功构建了一种高效、经济的脊椎动物抗衰老药物筛选平台。sapanisertib抗衰功能的发现不仅为早衰症患者提供了潜在的治疗方案,也为延缓衰老提供了全新的药物和机制。目前,sapanisertib作为抗癌药物已进入II期临床试验阶段,已完成的安全性数据和药代动力学研究有望加速其作为抗衰老药物的研发。
复旦大学生命科学学院/西南大学发育生物学与再生医学研究中心罗凌飞教授为该论文通讯作者,青年研究员马建龙和博士生陈杨为该论文共同第一作者。
编辑信箱
欢迎您推荐或发布各类关于实验动物行业资讯、研究进展、前沿技术、学术热点、产品宣传与产业资源推广、产业分析内容以及相关评论、专题、采访、约稿等。
我要分享 >热点资讯
- 年
- 月
- 周





