溶血是一个生理或病理情况下都可能发生的现象,比如输血过程,败血症,镰状细胞贫血等。溶血会在血液中产生大量游离血红蛋白(Hemoglobin,Hb)及其代谢产物非结合型胆红素(Unconjugated bilirubin,UCB),游离的Hb可能产生大量的活性氧造成组织损伤,并耗竭NO造成血管痉挛和系统性高压(1–3),而UCB的异常升高会导致高胆红素血症及黄疸。在严重的高胆红素血症新生儿中,游离的UCB进入脑区,可能会引起神经系统的不可逆损伤,甚至新生儿死亡(4, 5)。目前普遍认为血浆中游离的Hb主要由巨噬细胞清理,而UCB则由肝细胞代谢转化(5–8)。红细胞生成性卟啉病(Erythropoietic protoporphyria,EPP)是一种光诱导溶血的罕见遗传病,主要症状是皮肤光敏性和肝脏疾病(9)。该类病人的红细胞缺乏亚铁螯合酶(Ferrochelatase,FECH),因此原卟啉(Protoporphyrin IX,PPIX)生成血红素的反应受阻,导致机体堆积大量PPIX。PPIX在光刺激下能产生氧化应激反应,导致红细胞裂解以及组织损伤。虽然研究报道能在EPP模型小鼠的肝细胞,库普弗细胞(肝脏巨噬细胞)及胆小管中看到PPIX的沉积(10),但是其具体代谢清除机制还不清楚。
2025年2月11日,华南理工大学徐进教授团队、李飞飞副教授团队以及南方科技大学何思聪助理教授团队合作在PNAS上在线发表了题为“Scavenger endothelial cells alleviate tissue damage by engulfing toxic molecules derived from hemolysis”的研究论文。该研究发现清道夫内皮细胞的内吞功能在生理及病理性溶血过程中起保护性作用。
清道夫内皮细胞是一种能高效内吞血液中大分子废物的吞噬细胞,在脊椎动物中高度保守(11)。其主要分布在血流丰富的区域,例如哺乳动物的肝窦静脉内皮细胞,斑马鱼中尾部静脉和静脉丛细胞(12)。虽然多种外源注射进血液中的大分子,比如oxLDL,脂质体,纳米颗粒,多聚糖等等,都能被清道夫内皮细胞内吞,但对其内吞功能背后的生物学意义的理解还非常有限。清道夫内皮细胞强大的内吞能力和分布特性让研究者好奇它是否在溶血过程中有未被揭示的重要作用。
研究者首先在斑马鱼中显微注射荧光标记的Hb,天然橘黄色的UCB和结合型胆红素(conjugated bilirubin,CB)(在共聚焦显微镜微分干涉相差显示设定下为黑色颗粒),结果显示清道夫内皮细胞即静脉内皮细胞能内吞Hb和UCB,但不能内吞CB(图1)。利用苯肼(Phenylhydrazine,PHZ)诱导斑马鱼幼体急性溶血之后,负责血红蛋白降解的血红加氧酶(hmox1a,hmox1b)在静脉内皮细胞中的表达相比对照组的静脉内皮细胞中显著升高(图2),提示斑马鱼清道夫内皮细胞参与血红蛋白的代谢。
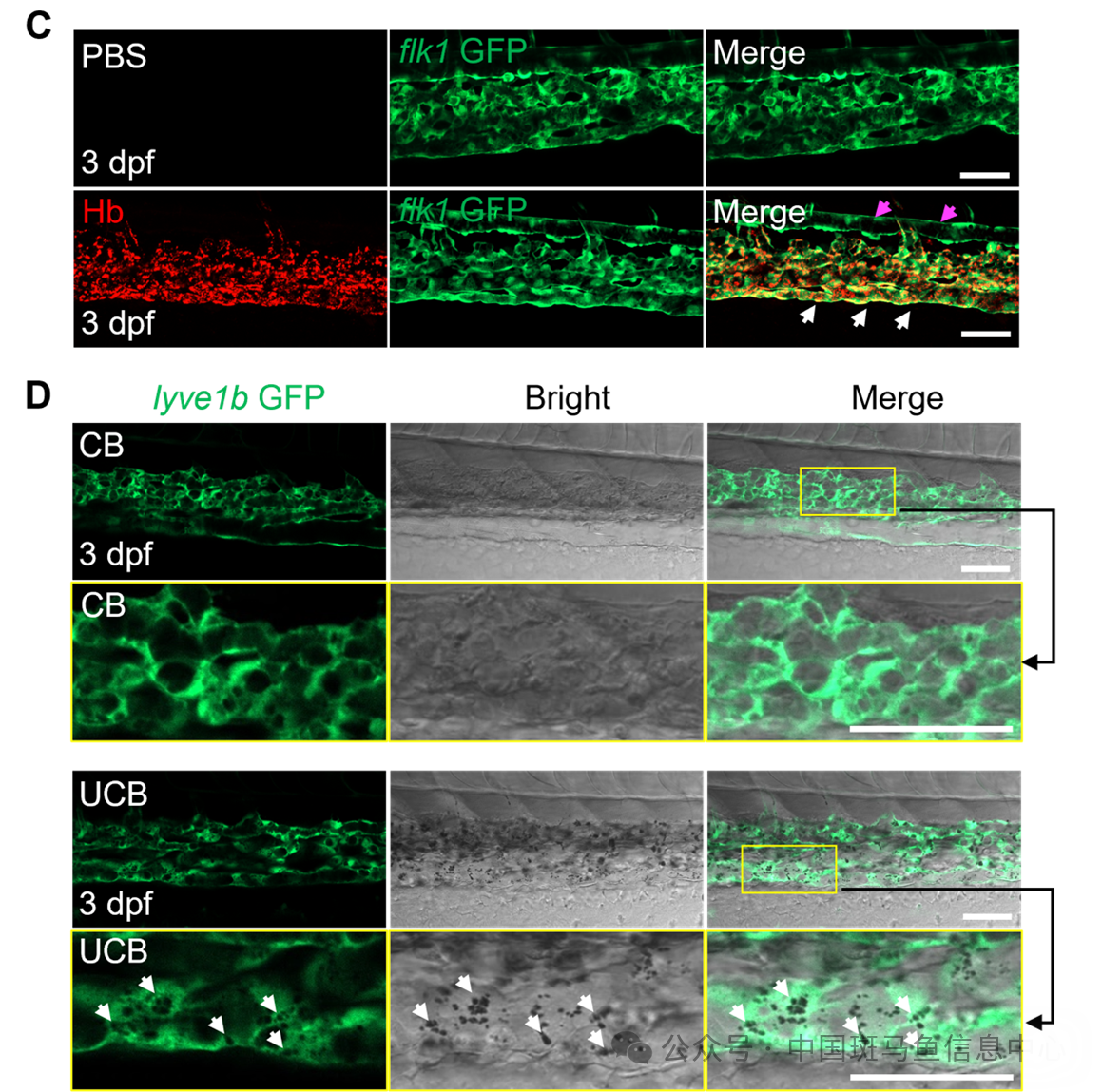
图1 清道夫内皮细胞内吞Hb和UCB
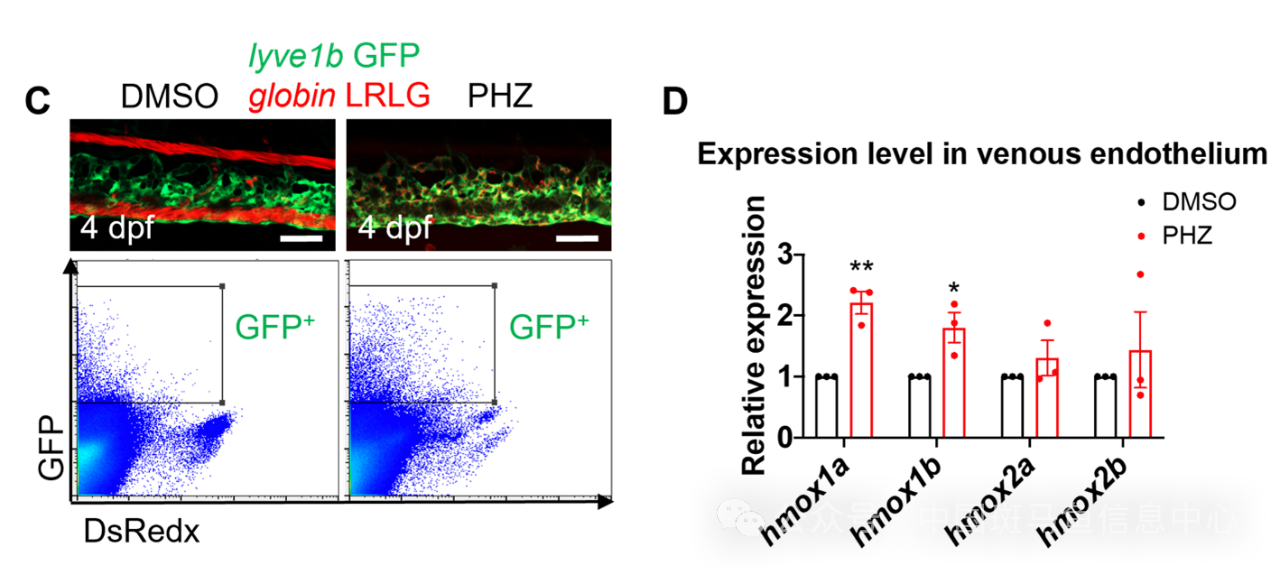
图2 清道夫内皮细胞在溶血情况下高表达hmox1a/1b
为了进一步探究清道夫内皮细胞在溶血过程中的作用,研究者通过CRISPR/Cas9建立了fech突变的EPP斑马鱼模型。利用PPIX的自发荧光属性及光谱特征,研究者发现光诱导溶血释放的PPIX也能被静脉内皮细胞内吞,并且这一过程依赖于清道夫受体Stab2(图3)。在stab2的突变体EPP斑马鱼的组织上清液中,PPIX的含量相比于对照组EPP斑马鱼的组织上清液中显著上升(图4A-C)。与此同时,stab2的突变体EPP斑马鱼在光照刺激下的存活率明显低于对照组EPP斑马鱼的存活率(图4D-E)。这些结果提示了斑马鱼清道夫内皮细胞在EPP溶血过程中通过吞噬清除PPIX来起保护作用。
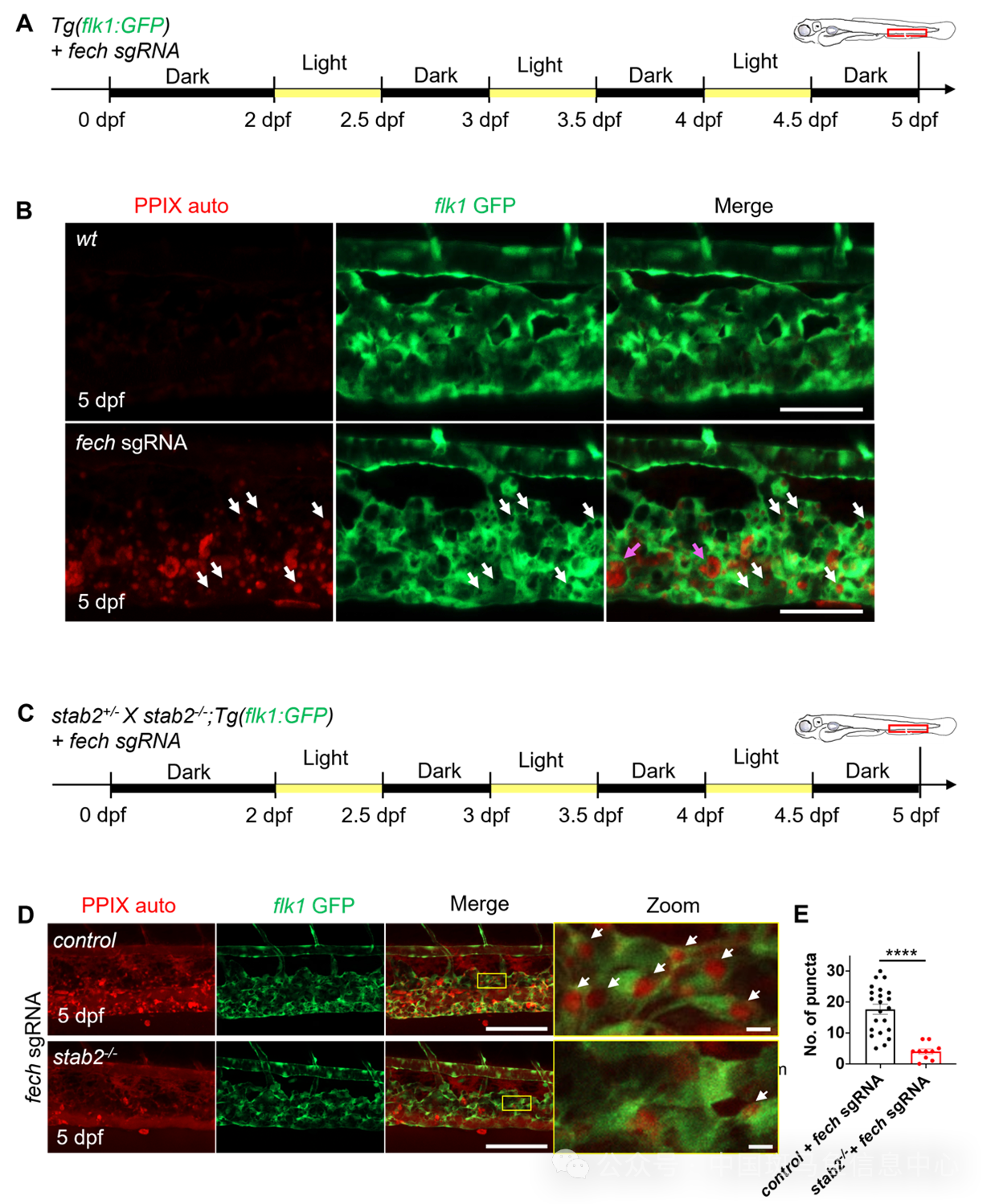
图3 清道夫内皮细胞通过Stab2内吞PPIX
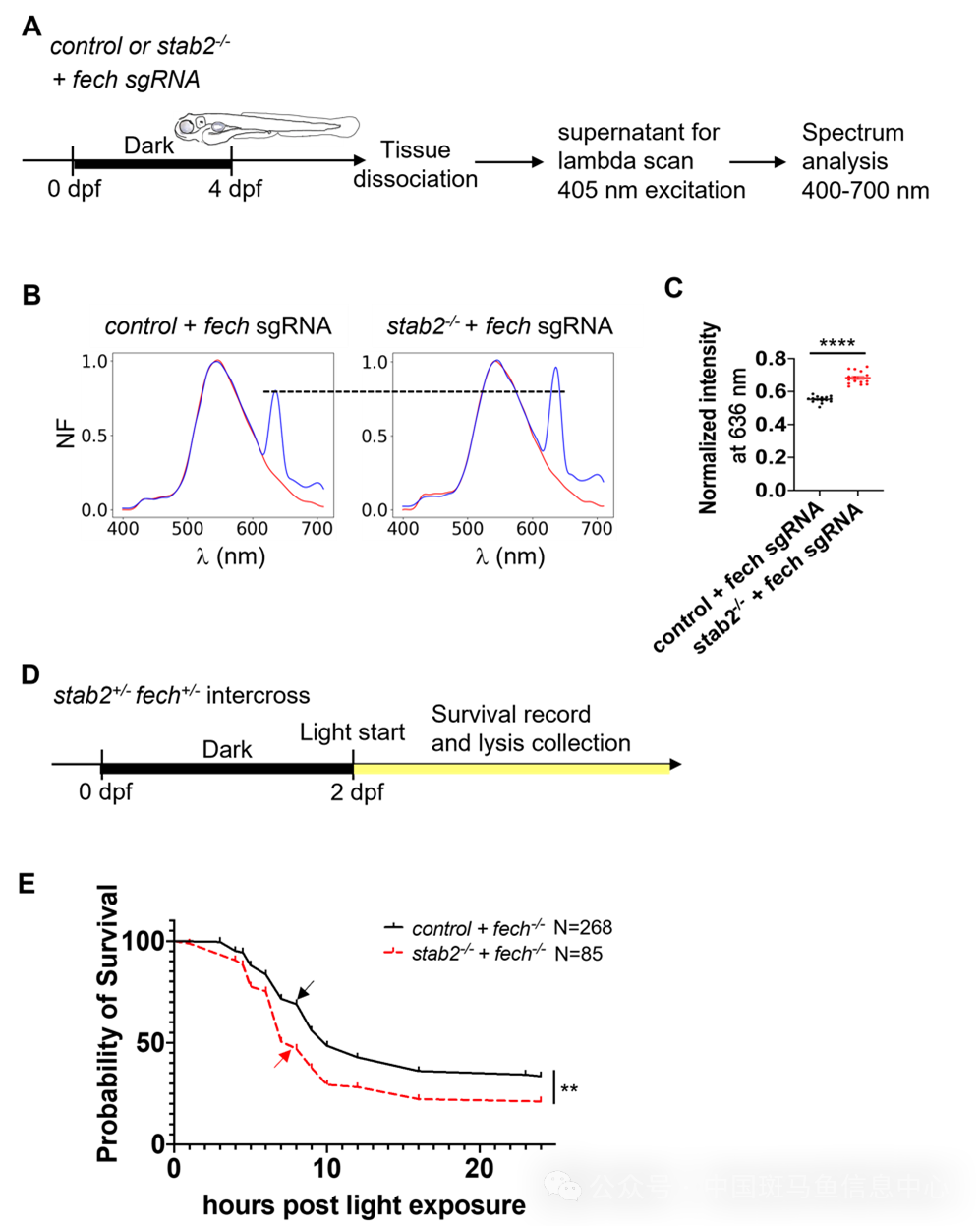
图4 清道夫内皮细胞在EPP模型中起保护作用
最后,研究者在小鼠中通过静脉注射Hb,UCB及PPIX验证了小鼠清道夫内皮细胞即肝窦静脉内皮细胞对这些分子的保守吞噬作用(图5)。

图5 小鼠清道夫内皮细胞可以内吞Hb、UCB和PPIX
华南理工大学医学院戴一梅博士和姜沄沄博士为本文的共同第一作者,华南理工大学医学院徐进教授,李飞飞副教授和南方科技大学何思聪助理教授为本文的共同通讯作者。本研究受到了广东省自然科学基金-卓越青年团队项目、科技部国家重点研发计划项目、国家自然科学基金以及广州市科技项目的支持。
1. D. J. Schaer, P. W. Buehler, A. I. Alayash, J. D. Belcher, G. M. Vercellotti, Hemolysis and free hemoglobin revisited: exploring hemoglobin and hemin scavengers as a novel class of therapeutic proteins. Blood 121, 1276–1284 (2013).2. J. S. Olson, et al., No scavenging and the hypertensive effect of hemoglobin-based blood substitutes. Free Radic. Biol. Med. 36, 685–697 (2004).3. J. W. Deuel, et al., Hemoglobinuria-related acute kidney injury is driven by intrarenal oxidative reactions triggering a heme toxicity response. Cell Death Dis. 7, e2064–e2064 (2016).4. J. Phillips, A. C. Henderson, Hemolytic Anemia: Evaluation and Differential Diagnosis. Am. Fam. physician 98, 354–361 (2018).5. T. W. R. Hansen, R. J. Wong, D. K. Stevenson, Molecular Physiology and Pathophysiology of Bilirubin Handling by the Blood, Liver, Intestine, and Brain in the Newborn. Physiol. Rev. 100, 1291–1346 (2020).6. J. R. Chowdhury, P. L. M. Jansen, E. B. Fischberg, A. Daniller, I. M. Arias, Hepatic Conversion of Bilirubin Monoglucuronide to Diglucuronide in Uridine Diphosphate-Glucuronyl Transferase-Deficient Man and Rat by Bilirubin Glucuronoside Glucuronosyltransferase. J. Clin. Investig. 62, 191–196 (1978).7. D. J. Schaer, et al., CD163 is the macrophage scavenger receptor for native and chemically modified hemoglobins in the absence of haptoglobin. Blood107, 373–380 (2006).8. M. Kristiansen, et al., Identification of the haemoglobin scavenger receptor. Nature 409, 198–201 (2001).9. A. Brun, S. Sandberg, Mechanisms of photosensitivity in porphyric patients with special emphasis on erythropoietic protoporphyria. J. Photochem. Photobiol. B Biology 10, 285–302 (1991).10. S. Lyoumi, et al., Protoporphyrin Retention in Hepatocytes and Kupffer Cells Prevents Sclerosing Cholangitis in Erythropoietic Protoporphyria Mouse Model. Gastroenterology 141, 1509-1519.e3 (2011).11. T. Seternes, K. Sorensen, B. Smedsrød, Scavenger endothelial cells of vertebrates: A nonperipheral leukocyte system for high- capacity elimination of waste macromolecules. Proc Natl Acad Sci USA 1–4 (2002).12. F. Campbell, et al., Directing Nanoparticle Biodistribution through Evasion and Exploitation of Stab2-Dependent Nanoparticle Uptake. ACS Nano 12, 2138–2150 (2018).










