刘峰团队在斑马鱼实验中揭示Wdr5介导的H3K4甲基化修饰通过维持基因组稳定性促进造血干祖细胞发育
在脊椎动物中,造血过程主要包括两个阶段:初级造血和次级造血[1]。其中,次级造血所产生的造血干祖细胞(hematopoietic stem and progenitor cells,HSPCs),在胚胎发育期间不断成熟、增殖和分化,进而为机体终身造血奠定基础[2]。在斑马鱼胚胎发育过程中,HSPC最早产生于主动脉-生殖腺-中肾(aorta-gonad-mesonephros,AGM)区,之后迁移至尾部造血组织(caudal hematopoietic tissue,CHT)进行扩增。在扩增过程中,基因组的稳定性对于HSPC增殖至关重要[1, 3]。然而,目前关于胚胎发育过程中HSPCs基因组稳定性的调控机制仍知之甚少。
组蛋白的翻译后修饰通常被称为“组蛋白密码”,这类修饰在协助细胞应对复制应激以及维持基因组稳定性等方面,发挥至关重要的作用[4-6]。其中,组蛋白H3第4位赖氨酸(H3K4)的甲基化修饰由赖氨酸甲基转移酶2(KMT2)家族成员和核心亚复合物 WRAD(Wdr5、Rbbp5、Ash2l和Dpy30)构成的甲基转移酶复合物催化完成(7)。H3K4甲基化修饰是一种影响基因表达和染色质结构的重要表观遗传标记,在细胞分化、组织器官发育以及疾病发生等多种生物学过程具有调控作用[8-10]。然而,H3K4甲基化修饰是否调控HSPCs基因组稳定性尚不清楚。
2025年3月20日,刘峰研究员团队在PNAS 杂志发表题为 “Wdr5-mediated H3K4 methylation facilitates HSPC development via maintenance of genomic stability in zebrafish”的文章,该研究揭示了Wdr5介导的H3K4甲基化修饰通过阻止R-loop结构的异常积累和促进DNA损伤应答(DNA damage response,DDR)信号通路激活,维持HSPC基因组的稳定性,进而促进HSPC发育。

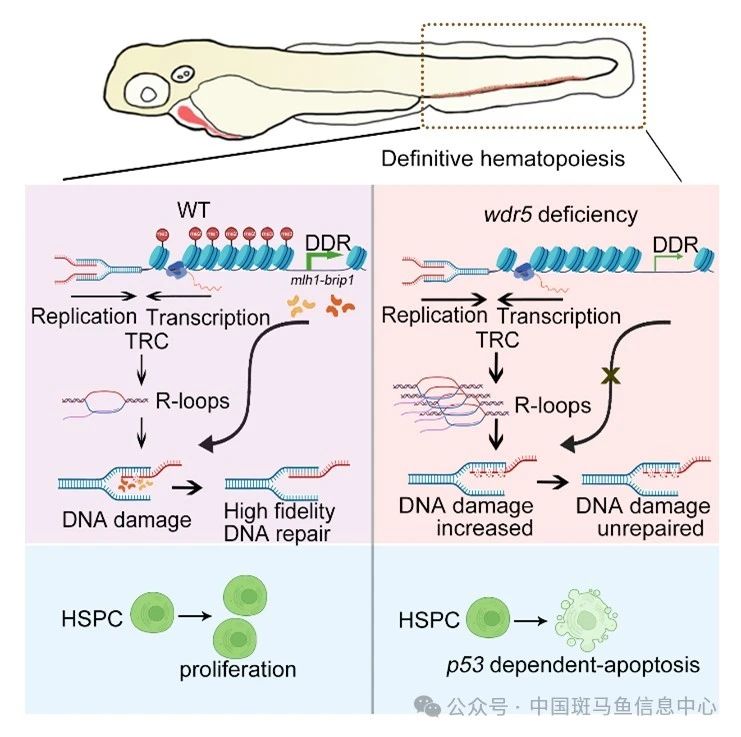
利用斑马鱼模型,研究人员首先发现wdr5在造血干细胞中表达。在斑马鱼wdr5突变体中,CHT区域HSPC数量减少,并且HSPC数量减少是由于p53依赖性细胞凋亡增加所致。为进一步研究wdr5调控HSPC发育的机制,研究人员通过碱基突变型和细胞特异性wdr5转录本过表达实验,发现Wdr5介导的H3K4甲基化修饰以细胞自主方式维持HSPC扩增。深入的机制探索发现,Wdr5介导的H3K4甲基化修饰能够抑制HSPC快速增殖过程中的异常R-loop形成,从而维持基因组稳定性。在斑马鱼wdr5突变体中,R-loop的异常积累导致DNA损伤增加。随后,研究人员通过CUT&Taq测序分析,发现斑马鱼wdr5突变体的HSPC中H3K4me3甲基化修饰水平降低,导致DDR信号通路的无法激活,抑制DNA损伤修复的进程,损害基因组稳定性。最后,研究人员通过DDR信号通路相关基因mlh1和brip1的过表达,挽救wdr5突变体中HSPC数量降低的表型。
综上所述,Wdr5介导的H3K4甲基化修饰通过抑制R-loop的异常积累以及确保DDR信号通路的激活,维持HSPC基因组稳定性,进而保障HSPC正常增殖。该研究从表观遗传调控角度丰富了HSPC发育过程中基因组稳定性的维持机制。
中国科学院动物研究所博士生王晓涵为第一作者,刘峰研究员为通讯作者。感谢中国医学科学院血液病医院(中国医学科学院血液学研究所)王璐研究员、清华大学孟安明院士、上海交通大学洪登礼教授和浙江大学陈军教授在实验技术和材料等方面的帮助。该研究得到了国家自然科学基金、国家重点研发计划以及中国科学院动物研究所自主部署项目资助。
编辑信箱
欢迎您推荐或发布各类关于实验动物行业资讯、研究进展、前沿技术、学术热点、产品宣传与产业资源推广、产业分析内容以及相关评论、专题、采访、约稿等。
我要分享 >热点资讯
- 年
- 月
- 周





