欢迎您推荐或发布相关实验技术、实验攻略、实验经验分享等。
Cell子刊:细菌利用病毒潜伏期建立CRISPR-Cas免疫
2025年03月27日
来源:生物谷
作者:
责任编辑:yjcadmin
摘要:在这项新研究中,研究团队证明了细菌通过利用温和噬菌体的另一种休眠(即“溶源”)生命周期来建立 CRISPR-Cas 免疫。
约翰·霍普金斯大学的研究人员在 Cell 子刊 Cell Host & Microbe 上发表了题为:Bacteria exploit viral dormancy to establish CRISPR-Cas immunity 的研究论文。
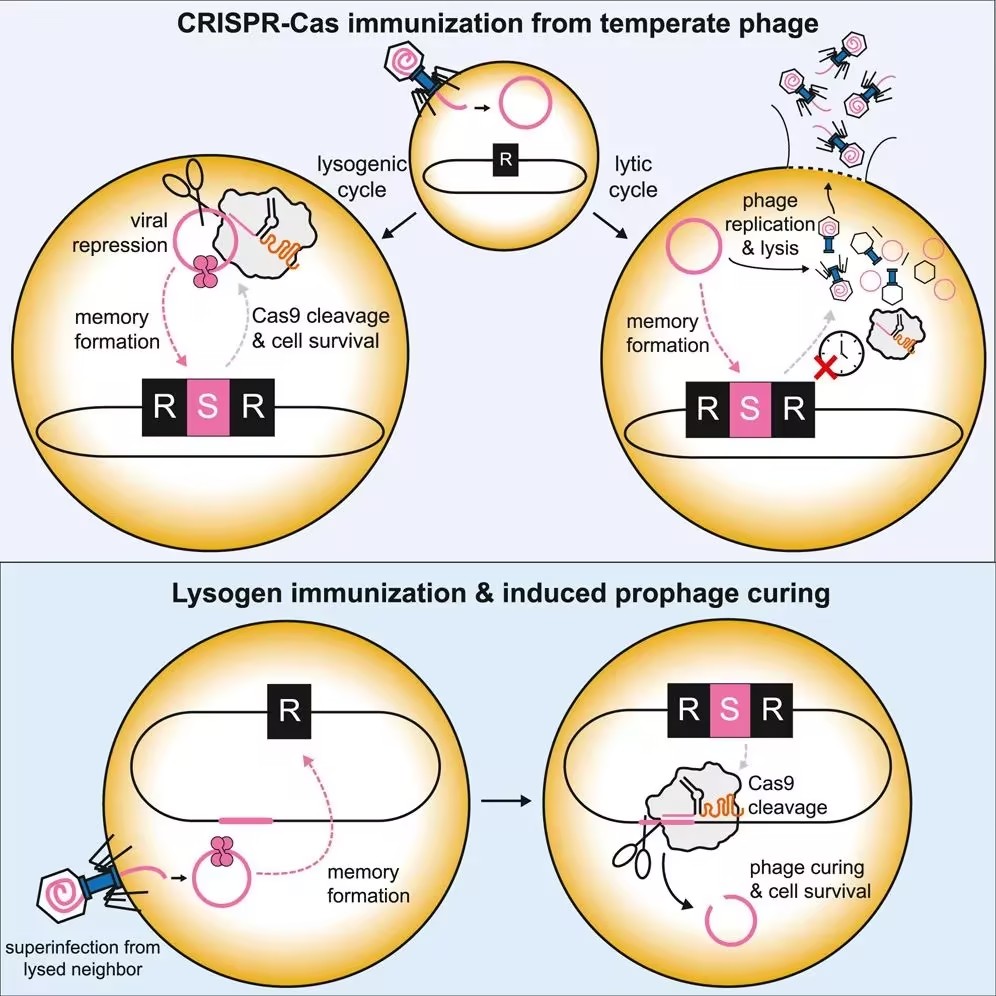
该研究表明,细菌利用病毒的潜伏期(噬菌体的溶源周期)来建立 CRISPR-Cas 免疫,也就是说,噬菌体在将自身基因组整合至宿主菌基因组的溶源周期中,细菌安全捕获其病毒 DNA 片段作为免疫记忆。

根据噬菌体和宿主菌的关系,可将噬菌体分为两类:一类噬菌体在宿主菌细胞内迅速增殖,产生许多子代噬菌体,并最终使宿主菌细胞破裂,这类噬菌体被称为烈性噬菌体( virulent phage);另一类噬菌体感染宿主菌后不立即增殖,而是将自身核酸整合到宿主菌染色体中,随宿主核酸的复制而复制,并随细胞的分裂而传代,这类噬菌体被称作温和噬菌体(temperate phage),也叫做溶原性噬菌体(lysogenic phage)。
在这项新研究中,研究团队证明了细菌通过利用温和噬菌体的另一种休眠(即“溶源”)生命周期来建立 CRISPR-Cas 免疫。
在噬菌体感染期间,进入溶源状态的细胞的免疫率显著高于发生裂解的细胞。此外,在没有外来威胁的情况下,细菌能够获得靶向染色体中潜伏噬菌体的间隔区。在这种情况下,Cas9 的自我靶向作用促进了前噬菌体(prophage)的治愈,使免疫细胞能够避免自身免疫。
在建立和维持溶源性过程中优先获取间隔区的现象,或许可以解释为何在天然细菌分离株中,大多数间隔区都靶向温和噬菌体的。
上一篇:狗狗情绪揭秘:人类误判背后的真相[ 03-26 ]
下一篇:灵长类动物非病毒基因传递系统出炉[ 03-28 ]