卵巢癌原位移植—转移动物模型
1.造模材料 动物:BALB/cnu/nu裸鼠,雌性,鼠龄4~5周,体重17~20g,在无特殊病原菌的条件下饲养;细胞:高转移卵巢癌细胞株HO-8910PM。已证实该细胞株的裸鼠皮下移植瘤和转移瘤保持原始人卵巢低分化浆液性囊腺瘤的形态学特性。
2.造模方法 原位移植瘤模型的建立:首先将HO-8910PM细胞悬液接种于裸鼠右肩胛区皮下,2×1000000个细胞/只,待皮下移植瘤长至1cm3时,脱颈处死裸鼠,无菌条件下切取新鲜癌组织,剪成1mm3组织小块,置冰磷酸盐缓冲液(PBS)中供移植用。原位移植术前裸鼠需禁食12h,1%氯胺酮(100mg/kg)麻醉后取右侧肋缘下背侧切口,打开腹膜后腔,暴露右侧卵巢,收拾显微镜下剪开卵巢外被包膜,用7-0无损伤缝合线将一枚1mm3瘤组织小块固定在卵巢表面,少许医用生物蛋白胶封闭包膜,逐层关腹,术后继续 SPF条件饲养。
原位移植瘤生长:本实验中共有16只裸鼠进行原位移植术,术后被随机分成A和 B两组,每组8只,每3天扪查腹部了解移植瘤的生长情况,观察裸鼠活动状态。移植术后第4周(28天),将A组鼠在1%氯胺酮(100mg/kg)腹腔注射麻醉下取腹正中切口打开腹腔,切除右侧卵巢及其移植瘤后缝合腹腔,与B组一同继续饲养。移植术后第11周(77天),将A、B组裸鼠同时脱颈处死。以游标卡尺测量肿瘤相互垂直的两条径线,分别记为X和Y,并计算平均肿瘤直径(MTD),MTD的计算方法为(xy)1/2。转移瘤生长:A、B两组裸鼠被处死后均进行系统解剖,观察各内脏和区域淋巴结转移情况,同时取肿瘤组织、盆腹腔脏器转移灶及淋巴结行常规病理(HE染色)和电镜检查。
3.造模后一般变化
(1)原位移植瘤生长情况:移植术后第3周起,在16只裸鼠右上腹部均可扪及米粒大小的肿瘤结节,质地较硬。A组裸鼠于原位移植术第4周切除右侧卵巢及移植瘤,并继续饲养,测量其移植瘤MTD为(4.7±1.0)mm。B组裸鼠为移植术后持续饲养观察,见上腹部肿瘤结节渐增大,至第8周时,均可扪及突出于腹部的肿块,活动度差,荷瘤裸鼠开始出现消瘦并逐渐加重,第11周时荷瘤裸鼠因腹部瘤体负荷过大,消瘦明显,呈全身衰竭状态,此时处死B组裸鼠,取其右侧移植瘤,测MTD为(13.2±2.8)mm,第4周(A组)和第11周(B组)裸鼠的右侧卵巢移植瘤MTD比较,差异有极显著性。本实验共对16只裸鼠进行原位移植,移植成瘤率为100%(16/16)。A组裸鼠第11周时无消瘦,无腹部膨胀,进食正常,处死后探查已切除的右侧附件区,未见有肿瘤继续生长。
(2)转移瘤生长情况:移植术后第11周,解剖发现,B组裸鼠右侧卵巢已被移植瘤组织替代,增大变形,呈圆形、椭圆形或不规则型,质地硬,切面见多个大小不等灰白色融合性团块,部分卵巢瘤体与腹壁和肠壁粘连;腹腔内多脏器表面呈现细颗粒状、结节状、大小不等团块状的灰白色转移灶,直径为0.2~0.8cm,多数种植在脏器表面,但部分向组织内浸润生长(由病理切片证实);转移发生部位分别为:对侧卵巢(5/8),盆壁腹膜(8/8),肠系膜(2/8),后腹膜(3/8),横膈(2/8),肠壁(6/8),肝表面(4/8),脾脏表面(2/8),肾脏(1/8),肺(1/8),淋巴结(4/8,共6枚,分别为髂内2枚、髂总2枚、腹主动脉旁1枚、腹股沟1枚);有2例腹腔内出现血性腹水2~3ml。本实验8组裸鼠原位移植卵巢癌的转移率为8/8,而A组裸鼠在第11周时与B组裸鼠被同时处死,但所有A组裸鼠体内未见肿瘤转移结节。
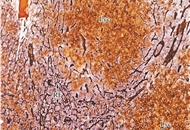
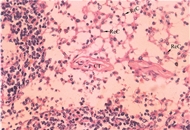
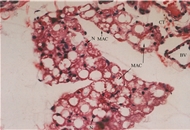
4.造模后病理变化 病理检查:光镜下见卵巢原位移植瘤组织细胞形态结构与各脏器转移瘤相一致,瘤细胞成片块状弥漫分布或排列成团状,细胞核大深染,细胞核与细胞质的比例大,分化程度低,呈浸润性生长;腹腔内各脏器如肝、脾和肠壁表面的种植转移瘤灶向组织内浸润生长,转移灶的癌组织结构及细胞形态与原位移植瘤相似;有1例裸鼠肺表面外观正常,但在连续切片时可见肺毛细血管内有转移性癌栓;转移的淋巴结除边缘部分残留少量淋巴组织外,整个淋巴结结构被癌细胞破坏和浸润。原位移植瘤和转移瘤在形态学和组织学上均与HO-8910PM细胞一致。透射电镜下见瘤细胞呈类圆形或不规则形,细胞表面被覆有指状突和丰富的微绒毛;细胞核大而异形,核仁增多、增大;细胞质有丰富的核蛋白体、微囊泡和扩大的粗面内质网池,可见分泌颗粒;另外,多个瘤细胞排列成类腺腔样结构及细胞表面丰富的微绒毛,均是浆液性肿瘤的特征结构。