南通大学刘东团队结合斑马鱼模型发现新的血管新生的负调控因子-GPR182
血管生成是指从已有血管形成新血管,其在胚胎发育以及肿瘤进展等过程中均发挥着重要作用。以肝癌为代表的高血管化肿瘤,往往展现出强烈的血管生成活性。此类过程主要受血管内皮生长因子(VEGF)、Notch Signaling以及血管生成素等因子的调控。鉴定新的血管新生调控因子不仅有助于理解心血管发生和形成的过程及其调控机制;而且也有助于找到心血管系统疾病的分子靶点,为治疗和预防缺血性疾病、代谢疾病及肿瘤等相关疾病提供新的思路和途径。
近日,南通大学刘东/陈昌盛团队在Angiogenesis.杂志在线发表一篇题为"G protein-coupled receptor GPR182 negatively regulates sprouting angiogenesis via modulating CXCL12-CXCR4 axis signaling"的研究论文,通过分析肝细胞癌病人组织样本特点,结合斑马鱼动物模型以及体外培养的血管内皮细胞实验验证,揭示了G蛋白偶联受体GPR182负调控血管新生的机制。

研究人员首先利用TCGA数据库中的公开数据,分析了肝细胞癌(HCC)患者中GPR182的表达水平。分析结果显示,在HCC患者中,GPR182的表达水平显著低于正常组织。此外,GPR182高表达与总体生存率(OS)和无病生存率(DFS)的提高呈正相关。在肝细胞癌组织中,GPR182 的表达水平显著降低,且与肿瘤血管密度呈现负相关。研究团队通过一系列实验发现,GPR182 在正常血管发育和病理状态下的血管生成中起着负调控作用。在模式生物斑马鱼胚胎中敲低 GPR182 的表达,会导致血管过度增生和异常血管网络形成,具体表现为血管芽生增多、血管分支复杂化等现象。此外,在体外实验中,敲低 GPR182 的人脐静脉内皮细胞(HUVECs)展现出更强的迁移和增殖能力以及管腔形成能力,这进一步证实了GPR182对血管生成的抑制作用。
研究进一步挖掘GPR182发挥作用的分子机制,发现 GPR182 能够通过与 CXCL12 结合,调节 CXCL12 的梯度,进而抑制 CXCR4 介导的血管生成信号通路。GPR182 作为一种特殊的“诱饵受体”,并不启动典型的 G 蛋白偶联受体信号转导,而是通过与 CXCL12 结合并促使其内吞和降解,降低 CXCL12 的生物可用性,从而削弱 CXCR4 信号的激活,最终抑制血管内皮细胞的迁移和增殖,控制血管新生的过程。
基于GPR182 在肝细胞癌中的低表达特征以及其对血管生成的关键调控作用,本研究为肿瘤治疗提供了新的思路。研究中使用 CXCR4 信号通路抑制剂 AMD3100 对 GPR182 缺陷的斑马鱼胚胎和肝细胞癌模型进行治疗,结果显示能够显著改善异常的血管新生表型,这为肿瘤的治疗提供新的策略和潜在的药物靶点。
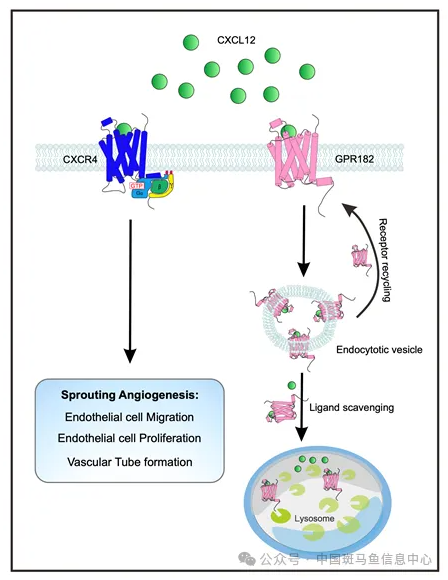
GPR182调控血管新生的机制
南通大学陈昌盛副教授、硕士研究生刘伟、袁芳以及王晓宁博士为论文的第一作者,南通大学刘东教授和陈昌盛副教授为论文的通讯作者。该研究获得了国家自然科学基金和江苏省自然科学基金等项目联合支持。
编辑信箱
欢迎您推荐或发布各类关于实验动物行业资讯、研究进展、前沿技术、学术热点、产品宣传与产业资源推广、产业分析内容以及相关评论、专题、采访、约稿等。
我要分享 >热点资讯
- 年
- 月
- 周





