周志刚/冉超团队揭示斑马鱼肠道菌群通过TLR2-嗜中性粒细胞-I型干扰素通路调控抗病毒免疫
脊椎动物肠道内存在大量共生细菌,肠道菌群在宿主的健康与疾病中发挥着至关重要的作用[1, 2]。过去十年里,研究揭示了肠道菌群在病毒感染中的调控作用[3–5]。尽管该领域已取得进展,我们对能够激活抗病毒免疫的共生细菌种类及潜在分子机制了解仍然有限。斑马鱼已成为研究脊椎动物-菌群互作的有力动物模型[6],其拥有与哺乳动物相似的免疫系统,且在生命早期完全依赖非特异性免疫[7]。与哺乳动物类似,病毒诱导的干扰素反应是斑马鱼抗病毒免疫的重要组成部分。鲤春病毒血症病毒(SVCV)是一种属于弹状病毒科的单链RNA病毒。由于斑马鱼对SVCV易感,斑马鱼-SVCV感染模型已被广泛用于硬骨鱼类抗病毒免疫的研究[8–10]。因此,利用斑马鱼模型开展“肠道微生物调控斑马鱼抗病毒免疫”机制研究,有着重要的理论意义和潜在应用价值。
2024年11月18日,周志刚/冉超团队在国际学术期刊Microbiome上发表了题为“The intestinal microbiome and Cetobacteriumsomerae inhibit viral infection through TLR2-type I IFN signaling axis in zebrafish”的研究论文。研究发现斑马鱼肠道菌群可通过TLR2-Myd88信号通路激活嗜中性粒细胞和I型干扰素(IFN)介导的抗病毒先天免疫,从而抑制病毒感染。进一步发现了肠道共生细菌索氏鲸杆菌(Cetobacterium somerae)与抗病毒表型高度相关,该菌复刻了肠道菌群通过TLR2-嗜中性粒细胞-I型干扰素通路调控抗病毒免疫的功能。此外,还发现索氏鲸杆菌的胞外多糖是与TLR2结合以激活I型干扰素反应的关键效应分子。

为研究肠道菌群在调控斑马鱼抗病毒免疫中的作用机制,研究团队首先利用无菌斑马鱼(GF)和二月龄斑马鱼抗生素饲喂(ABX)模型,发现GF和ABX组的死亡率和病毒载量显著高于有菌组,这提示肠道菌群可调控斑马鱼的抗病毒能力。为了探究菌群抗病毒作用的潜在机制,他们评估了无菌斑马鱼与有菌斑马鱼I型干扰素(IFN)反应。结果表明,斑马鱼肠道菌群对病毒感染后的I型IFN反应起重要调控作用。为了探究菌群对病毒感染的保护作用是否由I型IFN通路介导,他们使用CRFB1和CRFB2的在体反义寡核苷酸(vivo-MO)敲降I型IFN的受体,结果发现,CRFB1+2敲降消除了菌群的抗病毒作用,表明肠道菌群的抗病毒功能由I型IFN通路介导。除了I型IFN外,斑马鱼具有II型和IV型干扰素系统。为了探究II型和IV型IFN是否参与菌群介导的抗病毒反应,他们检测了SVCV感染后无菌和有菌斑马鱼中IFNγ、IFNγrel和IFNυ的表达。发现II型和IV型IFN的表达没有差异,这提示肠道菌群对病毒感染的保护作用不涉及II型和IV型IFN反应(图1)。
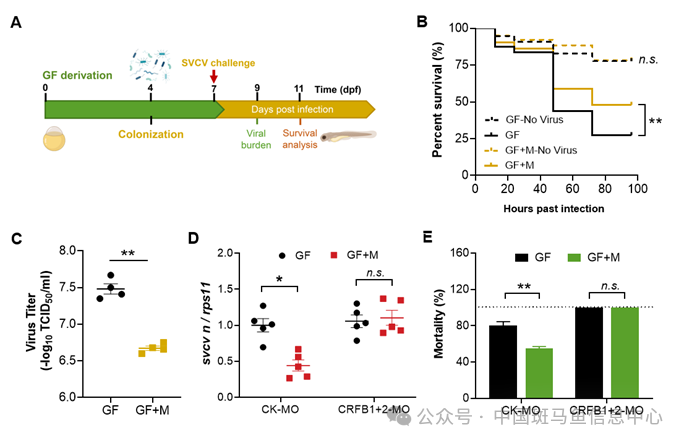
图1 肠道菌群调控斑马鱼抗病毒能力
进一步,他们研究了肠道菌群抗病毒作用中涉及的细胞免疫。在斑马鱼的幼鱼阶段,细胞免疫仅由髓系细胞组成,其中嗜中性粒细胞和巨噬细胞是主要的效应细胞。因此,首先评估了SVCV感染后无菌和有菌转基因斑马鱼品系Tg(mpx:EGFP) /Tg(mpeg1:EGFP) 中嗜中性粒细胞/巨噬细胞的募集和激活情况。结果发现SVCV感染后有菌斑马鱼的嗜中性粒细胞数量显著增加,无菌斑马鱼嗜中性粒细胞数量无显著差异。巨噬细胞在无菌和有菌斑马鱼中呈现相似的变化。与之对应,利用vivo-MO剔除嗜中性粒细胞可阻断肠道菌群的抗病毒功能,说明肠道菌群通过嗜中性粒细胞调控抗病毒免疫(图2)。
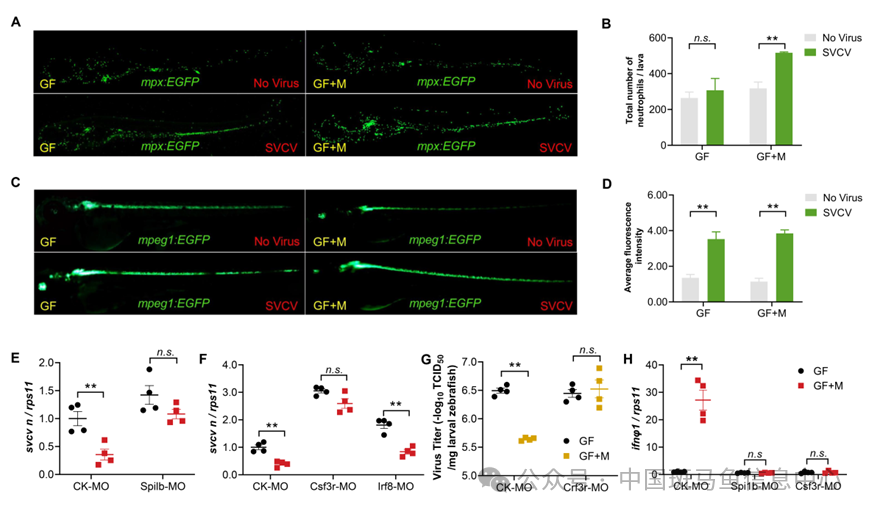
图2 肠道菌群通过嗜中性粒细胞发挥抗病毒功能
之后进一步研究了肠道菌群的抗病毒功能是否涉及模式识别受体。首先发现敲降Myd88基因可阻断肠道菌群抗病毒功能。Myd88是TLR的下游因子。通过敲降一系列的TLR受体,发现TLR2敲降可阻断肠道菌群的抗病毒表型,说明TLR2是介导肠道菌群抗病毒功能的核心受体。与抗病毒表型一致,TLR2敲降也阻断了肠道菌群对嗜中性粒细胞和I型IFN反应的激活。此外,结果显示肠道菌群的抗病毒功能不涉及TRIF因子,这说明肠道菌群不是通过TRIF通路直接激活IFN反应,而是通过Myd88通路对病毒诱导的IFN反应起到免疫增强的作用(图3)。
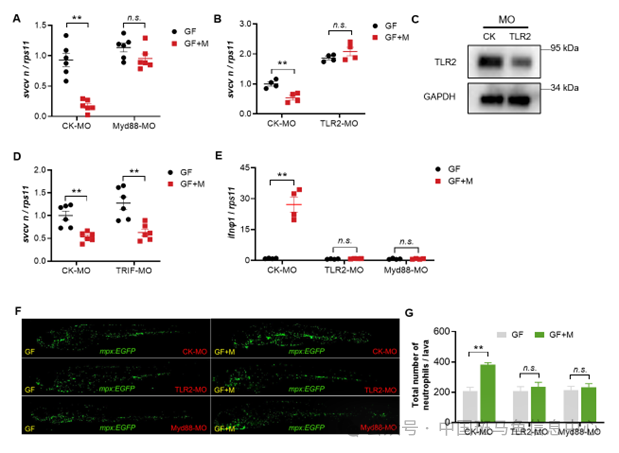
图3 肠道菌群抗病毒功能由TLR2-Myd88信号通路介导
为探究肠道菌群抗病毒的效应菌,研究者进一步进行了单抗生素饲喂,发现甲硝唑和克林霉素组的死亡率和混合抗生素组类似,而新霉素组的死亡率与对照组相似。随后对各组进行肠道菌群测序,发现鲸杆菌在高死亡率组别(混合抗生素组、甲硝唑组、克林霉素组)丰度极低,而在低死亡率组别(对照组、新霉素组)丰度未受影响。通过相关性分析发现鲸杆菌的丰度与肠道菌群的抗病毒功能高度相关,以此聚焦到效应菌-鲸杆菌。进一步研究发现鲸杆菌能发挥和肠道菌群类似的激活I型IFN和嗜中性粒细胞的功能,之后利用前期的技术手段研究了鲸杆菌的抗病毒机制。发现和肠道菌群类似,鲸杆菌的抗病毒功能由I型干扰素信号通路介导,并且依赖TLR2-Myd88通路和嗜中性粒细胞的功能(图4)。
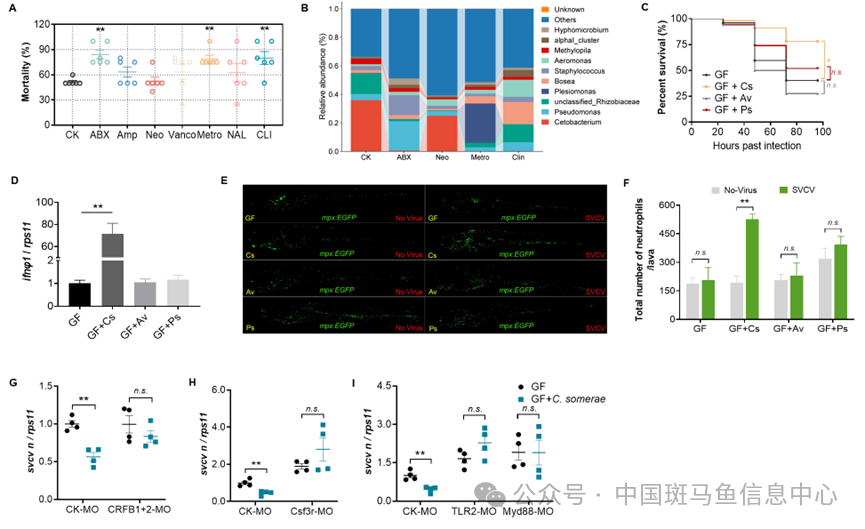
图4 鲸杆菌是肠道菌群抗病毒核心效应菌
最后也对鲸杆菌的抗病毒成分进行了探索。首先发现鲸杆菌培养物的上清液和菌体破碎物都具有抗病毒功能,并且发现抗病毒成分耐热,耐蛋白酶,且是一个大于3KD的生物大分子,因而推断活性成分是多糖。接着发现敲降TLR2可阻断鲸杆菌上清的抗病毒功能,而对鲸杆菌菌体破碎物的功能无影响,表明效应成分聚焦在上清液,提示是分泌性的胞外多糖发挥抗病毒功能。随后提取了鲸杆菌的胞外多糖,结果发现鲸杆菌胞外多糖具有抗病毒功能,其是与TLR2互作抑制病毒感染的效应分子,且抗病毒功能同样由I型干扰素通路介导。总之,该研究揭示了肠道菌群和鲸杆菌通过TLR2-Myd88-IFN通路调控斑马鱼抗病毒免疫的机制(图5)。
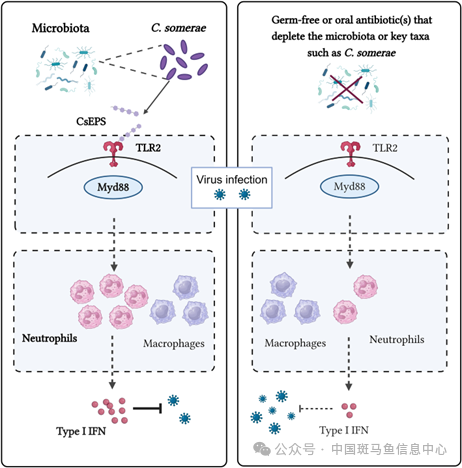
图5 肠道微生物调控斑马鱼抗病毒免疫通路图示
以上论文,中国农业科学院饲料研究所的周志刚和冉超研究员为通讯作者,梁慧博士生为第一作者,该项研究得到了国家自然科学基金和中国农业科学院科技创新工程的资助。
参考文献:1. Zhang B, Chassaing B, Shi Z, Uchiyama R, Zhang Z, Denning TL, et al. Prevention and cure of rotavirus infection via TLR5/NLRC4–mediated production of IL-22 and IL-18. Science. 2014;346:861–5.2. Stefan KL, Kim MV, Iwasaki A, Kasper DL. Commensal microbiota modulation of natural resistance to virus infection. Cell. 2020;183:1312–24.3. Monedero V, Collado MC, Rodríguez-Díaz J. Therapeutic opportunities in intestinal microbiota–virus interactions. Trends Biotechnol. 2018;36:645–8.4. Mazel-Sanchez B, Yildiz S, Schmolke M. Menage a trois: virus, host, and microbiota in experimental infection models. Trends Microbiol.2019;27:440–52.5. Ran C, Li Y, Ma XF, Xie YD, Xie MX, Zhang YT, et al. Interactions between commensal bacteria and viral infection: insights for viral disease control in farmed animals. Sci China Life Sci. 2021;64:1–12.6.Stagaman K, Sharpton TJ, Guillemin K. Zebrafish microbiome studies make waves. Lab anim. 2020;49:201–7.7. Lam SH, Chua HL, Gong Z, Lam TJ, Sin YM. Development and maturation of the immune system in zebrafish, Danio rerio: a gene expression profiling, in situ hybridization and immunological study. Dev Comp Immunol. 2004;28:9–28.8. Espín-Palazón R, Martínez-López A, Roca FJ, López-Muñoz A, Tyrkalska SD, Candel S, et al. TNFα impairs rhabdoviral clearance by inhibiting the host autophagic antiviral response. PLoS Pathog. 2016;12:1005699.9. Zhu J, Liu X, Cai X, Ouyang G, Zha H, Zhou Z, et al. Zebrafish prmt3 negatively regulates antiviral responses. Faseb J. 2020;34:10212–27.10. Lu LF, Jiang JY, Du WX, Wang XL, Li ZC, Zhou XY, et al. Fish female-biased gene cyp19a1a leads to female antiviral response attenuation between sexes by autophagic degradation of MITA. PLoS Pathog.2022;18:1010626.
编辑信箱
欢迎您推荐或发布各类关于实验动物行业资讯、研究进展、前沿技术、学术热点、产品宣传与产业资源推广、产业分析内容以及相关评论、专题、采访、约稿等。
我要分享 >热点资讯
- 年
- 月
- 周





