水生所夏晓勤团队揭示中草药苦玄参在水产模式动物斑马鱼中缓解代谢性炎症的机理
近日,中国科学院水生生物研究所夏晓勤团队在Water Biology and Security在线发表了题为“The effects ofPicria fel-terrae Lour. on ameliorating hepatic metaflammation while modulating mucosal immunity in fish”的研究论文,该研究揭示了中草药苦玄参在水产模式动物斑马鱼中缓解代谢性炎症的机理。

苦玄参 (Picria fel-terrae Lour.)作为一种传统的清热解毒、消肿止痛的草药,在模式鱼类斑马鱼肠肝炎症模型中,被证明对肠肝炎症起免疫调节和代谢调节的作用,还在鳃黏膜中发现长期抗炎效应。
苦玄参及其提取物对多种病原细菌有抑制作用,可预防和治疗水产动物的败血症、肠炎、烂鳃等细菌性疾病,但是还未应用于非病原菌引起的代谢性炎症及肠炎的预防。本研究中,3月龄斑马鱼饲喂含量为0.1%苦玄参6周后,肠绒毛形态与鱼粉对照组一致,而区别于豆粕组中绒毛萎缩;同时AB-PAS染色结果表明,苦玄参组杯状细胞数量多于豆粕组,提示苦玄参对黏膜屏障的保护作用。进一步,采用荧光标记免疫细胞的成像、流式细胞术和免疫荧光等方法,还发现中心粒细胞(幼鱼)、巨噬细胞(幼鱼和成鱼)和T细胞(幼鱼和成鱼)在肠粘膜的炎性聚集,苦玄参组较豆粕组表现为显著减少,揭示了苦玄参抗肠炎的细胞学机理。
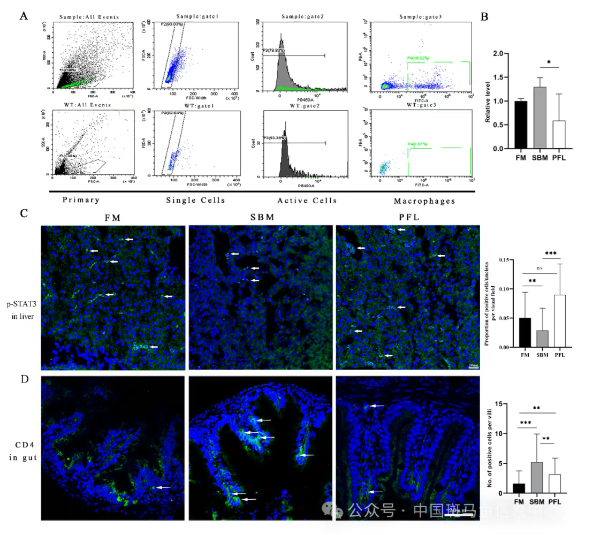
图1 苦玄参饲添对肠黏膜中巨噬细胞和T细胞的炎性聚集的抑制
为了进一步系统研究苦玄参饲料添加的肠肝保护效应,研究团队进行了转录组深度分析。苦玄参组与豆粕组相比,肠中差异表达基因(DEG)的富集分析显示,上调的主要为肠上皮更新有关的有丝分裂周期、DNA复制等过程;下调的则与白细胞趋化、溶酶体通路及跨膜转运活性等炎性过程相关。热图分析表明苦玄参组Treg/Th17相关基因(foxp3a、il22、il17a/f3)及促炎基因nfkb1表达下调。基于转录组的免疫细胞浸润分析还显示,苦玄参组肠中,静息NK细胞与活化记忆CD4⁺ T细胞减少,而单核细胞、静息肥大细胞、M2巨噬细胞和记忆细胞增多,暗示启动免疫调节功能。而在肝脏中,与豆粕组相比,苦玄参组上调的主要在脂代谢(长链脂肪酸和单羧酸的代谢),而下调的为细胞因子与受体互作、低氧(FoxO信号)有关通路,提示苦玄参促进肝脏脂代谢、抑制炎症、抗氧化的作用。
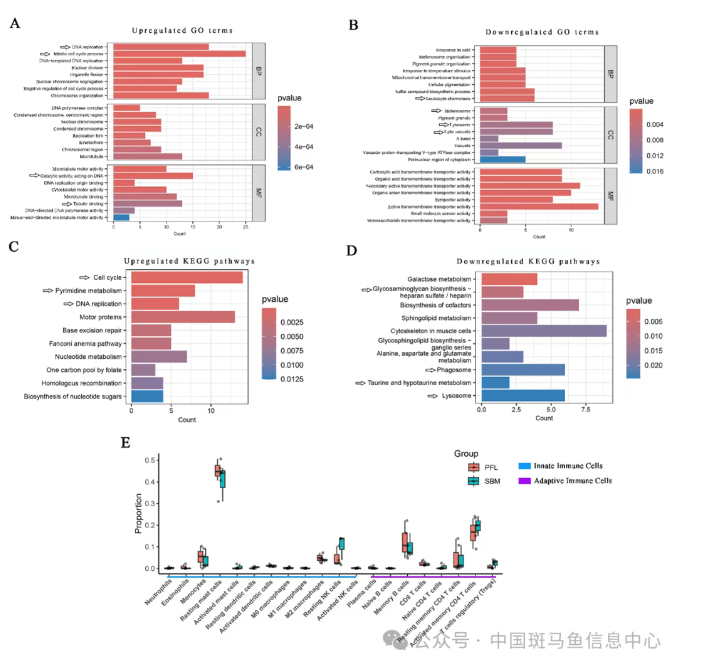
图2 3月龄斑马鱼肠的转录组水平(苦玄参组vs豆粕组)的深度分析
然后,采用SymMap和SwissTargetPrediction数据库进行了网络药理学分析。结果表明,苦玄参的活性成分对应到人类靶基因,与GeneCards中炎症性肠病(IBD)相关靶基因的共同靶点,再经同源转换找出与目前DEGs重叠的核心靶基因,进行富集分析,显示苦玄参干预IBD的生物学过程包括“细胞因子介导的信号通路”、“先天免疫应答”及“通过JAK-STAT的信号通路”等,并在分子功能中体现为蛋白酪氨酸激酶活性。同时,KEGG通路分析还揭示了Toll样受体、NOD样受体、RIG-I样受体、C型凝集素受体等免疫相关通路,以及MAPK、PPAR、mTOR、Wnt、胰岛素等代谢相关通路。因此,苦玄参通过靶向调节免疫应答核心通路及代谢相关信号网络来缓解鱼类肠炎。
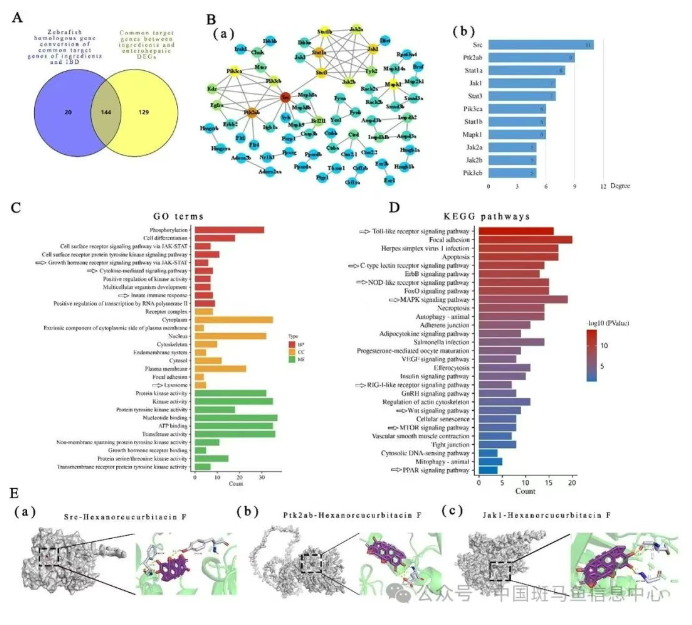
图3 网络药理学分析药物起效机理、核心成分及靶点基因
在靶点基因中,非受体酪氨酸激酶(src)、蛋白酪氨酸激酶2ab(ptk2ab)以及信号分子stat1a、jak1和stat3位列前五。为了揭示苦玄参药效的核心成分与靶蛋白的潜在结合,采用SwissModel模拟了蛋白结构,通过分子对接评估了己降葫芦素F与相关蛋白的结合能力。
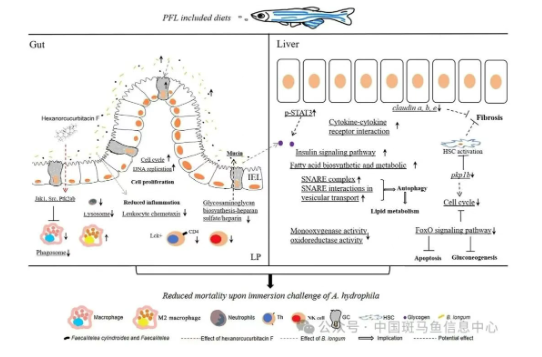
图4 饲添苦玄参缓解鱼类食源性肠炎及肝脏代谢性炎症的假设机制
综上,苦玄参可通过增加益生菌的丰度、促进肠上皮增殖、抑制肠黏膜免疫细胞的炎性聚集及促炎反应,来缓解鱼类食源性肠炎。在饲料中添加苦玄参还可恢复肝脏脂质和糖原代谢,缓解代谢性肠炎。苦玄参的主效成分己降葫芦素F,可能通过与巨噬细胞功能相关的蛋白质结合来发挥抗炎、抗菌作用。此外,苦玄参饲料添加的长期效应还表现为改善鳃黏膜免疫和对细菌感染的抵抗力。
编辑信箱
欢迎您推荐或发布各类关于实验动物行业资讯、研究进展、前沿技术、学术热点、产品宣传与产业资源推广、产业分析内容以及相关评论、专题、采访、约稿等。
我要分享 >热点资讯
- 年
- 月
- 周





