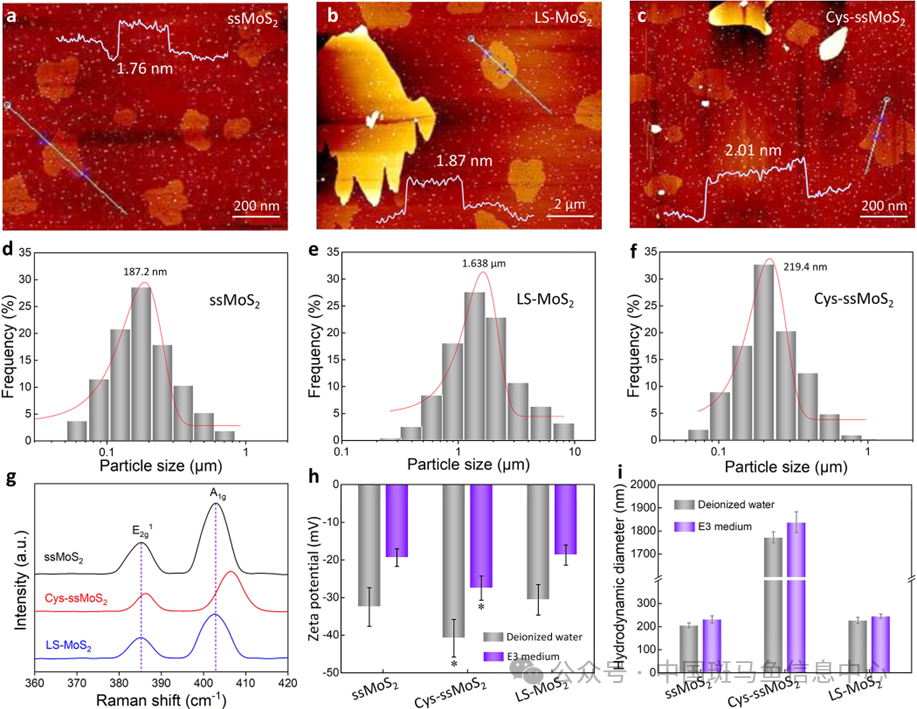
早期发育阶段的斑马鱼基于其生物敏感性极易受外源污染物干扰,心脏作为斑马鱼最早发育的器官之一,其结构功能的发育异常与外源污染物的暴露息息相关。单层MoS2是当前备受瞩目和极具应用价值的二维纳米材料之一,在其生产、使用、处理处置过程中存在环境释放和生物暴露的风险,系统评估其生态风险对于相关纳米废物的危害评估和纳米产业的可持续发展至关重要。然而,有关单层MoS2对水生脊椎动物的心脏毒性作用及机制还极少见报道,尤其是贴近环境相关条件下的低剂量暴露。2024年11月26日,河南师范大学环境学院邹威副教授和南开大学周启星教授在环境科学领域权威期刊Environmental Science & Technology在线发表题为“ MoS2 Nanosheets at Low Doses Induced Cardiotoxicity in Developing Zebrafish via Ferroptosis: Influence of Lateral Size and Surface Modification”的研究论文,基于120 h的斑马鱼(Danio rerio)胚胎毒性暴露实验,比较研究了不同尺寸和修饰前后的单层MoS2对斑马鱼幼鱼心脏发育的影响及机理。首次发现非致死剂量(0.5−100 μg/L)小粒径单层MoS2暴露诱发斑马鱼幼鱼明显的心脏毒性,基于转录组学、蛋白免疫印迹、荧光定量PCR阐释了MoS2通过激活细胞铁自噬和抑制铁转运蛋白FPN1活性诱发细胞铁死亡,诱发下游心肌肥厚细胞通路上调,导致斑马鱼心脏形貌结构发育畸形和泵血功能异常的分子途径。同时,研究人员集成共聚焦显微成像、高光谱原位观察、分子动力学模拟技术从纳米材料生物富集与纳米-蛋白互作角度揭示了颗粒尺寸和分子修饰在MoS2诱发斑马鱼铁死亡和心脏发育毒性的关键作用。该研究有助于深入理解单层MoS2致毒机制及其毒性构-效关系,为过渡金属硫化物纳米材料的设计及环境应用提供了重要支撑。实验首先对不同尺寸和修饰前后的MoS2纳米材料进行表征。基于AFM表征和数据统计显示,三种MoS2(ssMoS2, LS-MoS2, Cys-ssMoS2)形貌上均为单层片状结构,纳米片尺寸分别为187.2 nm,1.638 μm和219.4 nm;拉曼光谱、XPS结果证实半胱氨酸Cys分子主要与1T相MoS2的表面S原子结合,并显著增强其在去离子水和E3培养基中的分散性和胶体稳定性(图1)。
初期的预实验发现,较高浓度的小片径MoS2纳米片(ssMoS2,1和5 mg/L)暴露引发斑马鱼幼鱼严重的骨骼畸形甚至死亡,而非致死浓度(0.5−100 μg/L)的暴露时畸形表型则以心包囊肿为主(最高达22.3%),大片径MoS2纳米片(LS-MoS2)和Cys修饰后的纳米片(Cys-ssMoS2)暴露未观察到类似效应。H&E结果显示,ssMoS2暴露下的斑马鱼心室壁变薄、心房变窄,转基因斑马鱼Tg(myl7:eGFP)图片也显示暴露下的心脏结构呈弦状伸长,相比于空白组,100 μg/L ssMoS2处理组中斑马鱼SV-BA距离上调39.2%;此外,心脏TEM观察发现,低浓度ssMoS2暴露后出现明显的线粒体肿胀、肌纤维紊乱和肌节变长(最长达2.12 μm),这表明ssMoS2暴露引起鱼体心脏结构紊乱和心肌肥厚(图2)。
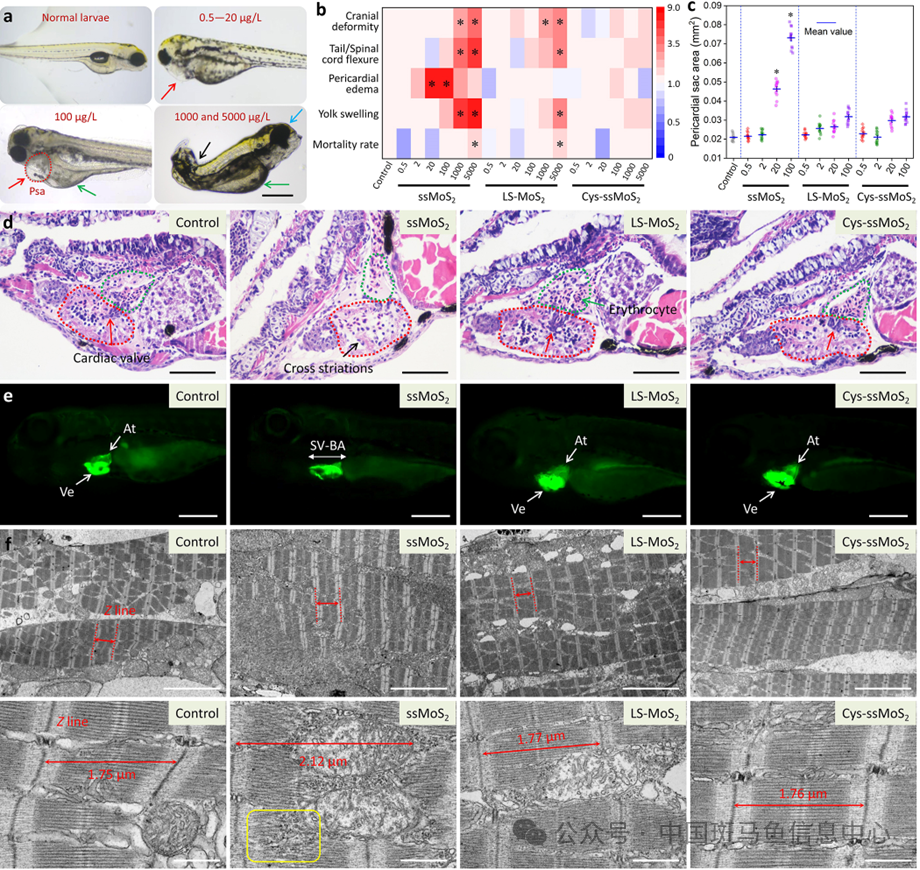
图2 暴露96 hpf的斑马鱼心脏形貌结构观
心脏功能评估结果发现,暴露于20和100 μg/L ssMoS2的幼鱼心跳次数显著下降,每搏输出量、心输出量和左室短轴缩短率均明显降低,相比之下,暴露于LS-MoS2和Cys-ssMoS2的斑马鱼心脏功能指标的变化微乎其微;邻联茴香胺染色结果显示,与对照组相比,暴露于ssMoS2后, 20和100 μg/L处理组中心脏红细胞数量分别减少32.8%和57.3%。上述实验结果表明小尺寸的单层MoS2低剂量暴露可诱发斑马鱼幼鱼心脏功能障碍(图3)。
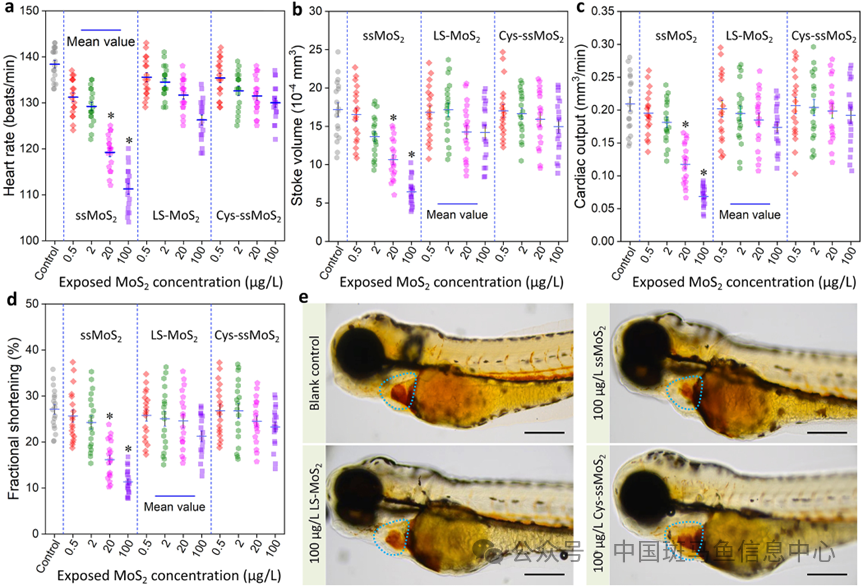
图3 96 hpf的斑马鱼心脏功能评估
进一步利用荧光标记、高光谱原位成像和质谱定量研究三种纳米片在斑马鱼体内的转运和生物富集。48 hpf的胚胎成像发现,ssMoS2和Cys-ssMoS2可穿透绒毛膜进入胚胎内部,而LS-ssMoS2尺寸大于绒毛膜孔(< 1 μm),无法转运进入胚胎;72 hpf的幼鱼成像发现,ssMoS2和Cys-ssMoS2出现在皮肤、鼻子、心脏和肌肉组织中,并且随着纳米片暴露浓度的增加,心脏区域的相对荧光强度也随之增加,而LS-MoS2主要分布在皮肤和鼻腔区域,在心脏部位未观察到明显荧光。利用高光谱成像观察也显示,ssMoS2和Cys-ssMoS2处理组幼鱼心脏组织中确实匹配到纳米颗粒,LS-MoS2处理组中则未检测到信号。ICP-MS结果显示,100 μg/L的ssMoS2和Cys-ssMoS2暴露组中整个幼鱼(分别为12.95和8.632 μg/mg tissue)和心脏区域(分别为3.774和1.951 μg/mg tissue)的纳米片富集量要明显高于LS-MoS2(分别为4.987和0.356 μg/mg tissue)。相比于原始ssMoS2,稳定性和分散性较好的纳米材料更易从生物体中清除,这可能是Cys-ssMoS2体内富集量偏少原因。此外,我们对可溶性Mo离子的暴露影响和胚胎氧含量进行分析并排除了相关影响,证实单层MoS2诱发斑马鱼心脏毒性需要其转运定位到心脏部分(图4)。
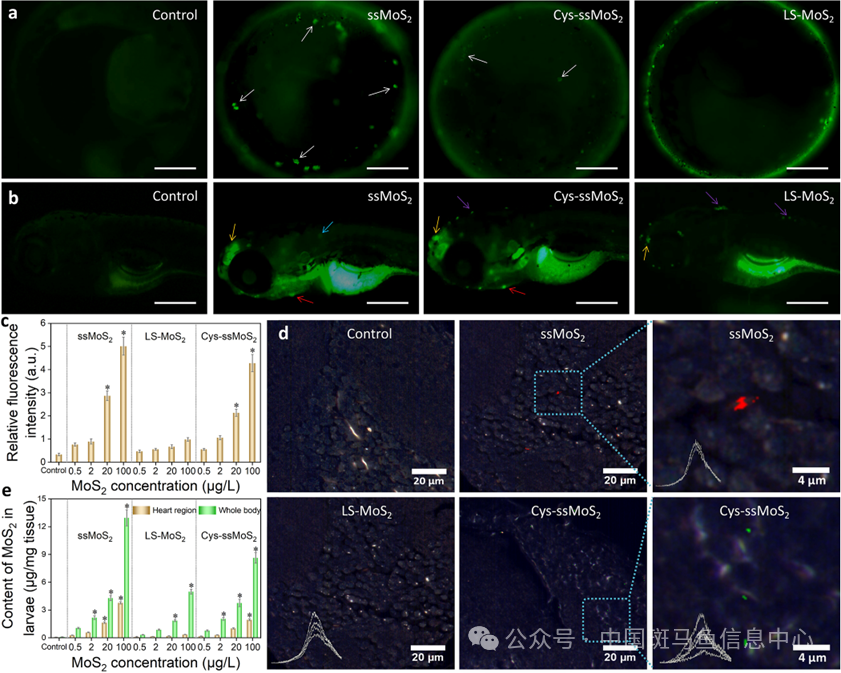
转录组学测试结果显示,暴露于100 μg/L的ssMoS2、LS-MoS2和Cys-ssMoS2后分别筛查出1616、969和807个差异表达基因,KEGG通路富集分析发现,ssMoS2和LS-MoS2均激活了外源物质降解和免疫系统,但是ssMoS2暴露特异性地激活了铁死亡和心肌肥大相关通路,而LS-MoS2组的差异基因主要与营养消化和吸收有关;Cys-ssMoS2处理组的斑马鱼显著受影响的过程主要与环境适应、感官功能和免疫系统有关。鉴于铁死亡是心血管相关疾病的发生的主要病理因素,我们进一步对铁死亡的关键事件进行验证分析。荧光FerroOrange探针染色和Fe2+定量分析结果显示,与LS-MoS2和Cys-ssMoS2组相比,ssMoS2处理组中幼鱼心脏区域观察到Fe2+富集量显著增加。还原性Fe2+的累积通过芬顿反应催化产生ROS导致氧化还原失衡,对应地,心脏ROS水平和MDA含量均明显上升,GPX4酶活性被显著抑制,相关性分析结果表明暴露于ssMoS2后诱发的铁死亡标志事件与心脏指标之间存在显著的相关性(r ≤ -0.78或 ≥ 0.78)。铁死亡抑制剂实验结果显示,加入5 μM Fer-1共暴露时,ROS、MDA和脂质过氧化恢复至正常水平,ssMoS2诱导的心脏异常和功能障碍也显著减轻。上述结果证实,ssMoS2暴露通过诱发铁死亡导致斑马鱼心脏发育异常,而Cys修饰可缓解其诱发的铁死亡效应和心脏毒性(图5)。
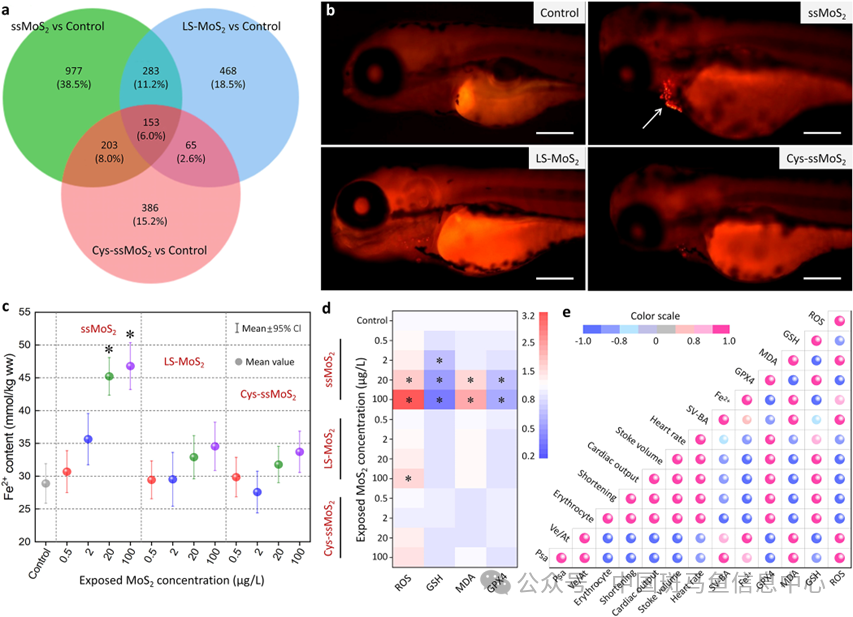
图5 铁死亡介导斑马鱼心脏发育毒性的预测与验证
利用100 μg/L的ssMoS2暴露斑马鱼120 h后,LC3和ATG5的蛋白水平分别比对照组高2.376和1.982倍,而储铁蛋白FTH的水平显著下调,转录组和定量PCR也检测到相关基因(map1lc3a、atg5和fth1b等)水平的显著变化,表明由ssMoS2暴露引起的过度铁蛋白自噬是导致心脏铁过载的重要因素。铁转运蛋白FPN1是脊椎动物唯一将细胞内Fe2+排出细胞的膜蛋白,本实验发现,转铁蛋白(tfa)及其相关受体(tfr1a和tfr1b)的mRNA表达水平未出现明显变化,表明ssMoS2暴露对铁转运进入细胞过程的影响微乎其微,然而ssMoS2显著抑制了FPN1蛋白水平,表明ssMoS2可以阻碍细胞内Fe2+的转出和外流。分子动力学模拟的结果也显示,ssMoS2纳米片可与FPN1蛋白结合并显著改变其二级结构,Cys修饰后的结构损伤明显减弱。此外,GSH代谢和磷脂合成的异常也参与ssMoS2诱发的心脏细胞铁死亡(图6)。
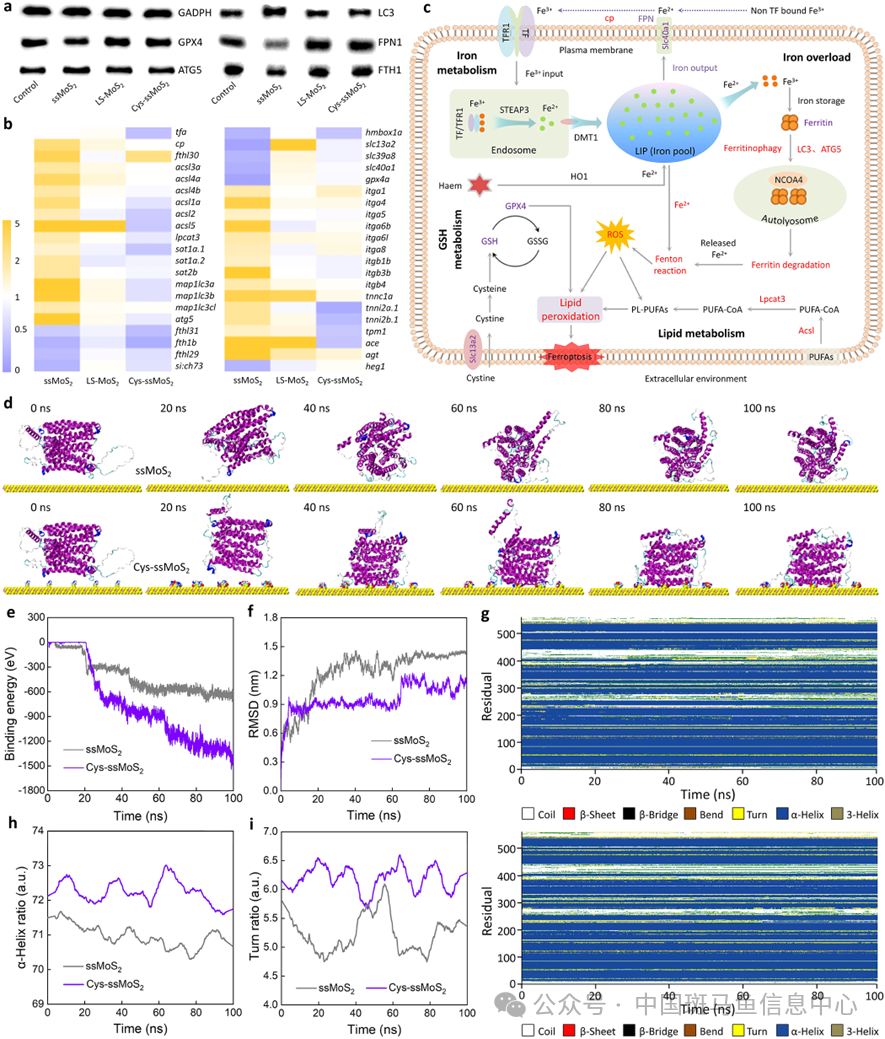
图6 铁死亡路径解析与分子动力学模拟验证
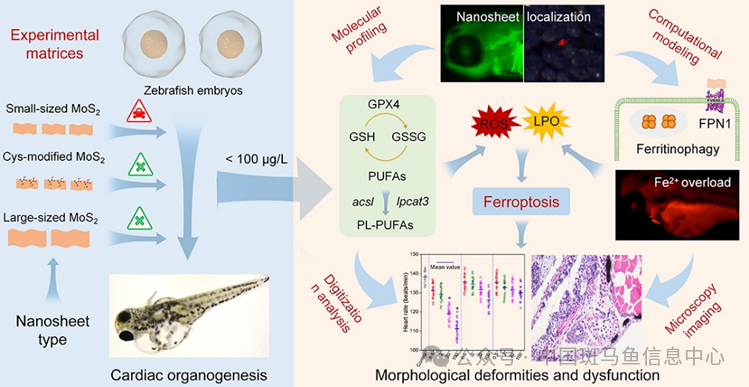
综上,这项工作揭示了小片径单层MoS2通过诱发细胞过渡铁自噬和抑制铁转运蛋白FPN-1活性促进Fe2+的胞内积累,同时引发GPX4表达下调和不饱和脂肪酸酯化增强,进而导致心脏出现铁死亡和显著心肌细胞损伤的潜在分子机制。修饰后的纳米片对膜铁转运蛋白的结构损伤和铁死亡效应显著减弱,显著缓解对斑马鱼的心脏毒性(图7)。通过对单层MoS2纳米片诱发心脏毒性的构-效关系与分子机理研究,可为后续研究环境相关浓度下TMDs的生态毒理效应提供借鉴和参考,为二维TMDs纳米材料的合成设计与安全应用提供科技支撑。
河南师范大学环境学院邹威副教授和南开大学周启星教授为本研究的通讯作者,邹威为本研究的第一作者。该研究得到了国家自然科学基金、河南省优秀青年科学基金的资助。









