李礼/赵方莹团队研究揭示斑马鱼Tango6-Rpb2信号轴调控造血干/祖细胞扩增的分子机制

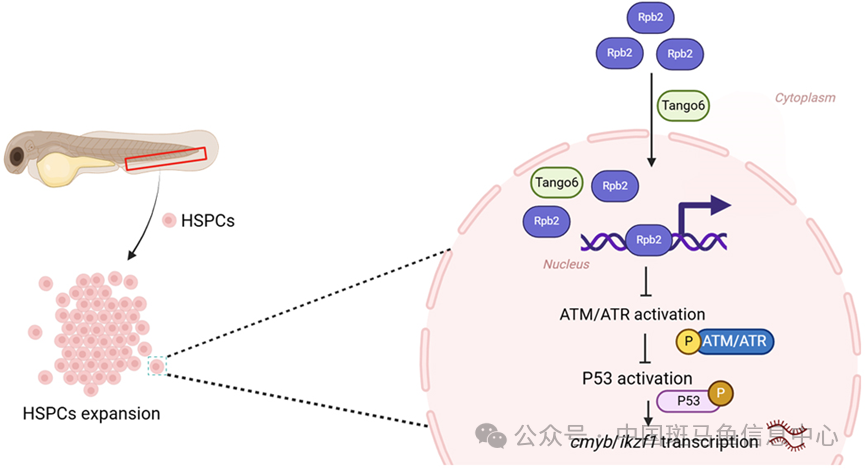
该团队前期揭示TANGO6通过COPI囊泡介导RPB2核转运是驱动细胞增殖的关键,且该信号轴对于小鼠HSCs的扩增不可或缺[5]。但Tango6-Rpb2轴调控HSPCs扩增的分子机制仍不清楚。该研究通过基于斑马鱼幼鱼的ENU正向遗传筛选,获得一个尾部造血组织(CHT)区域HSPCs增殖减少且永久造血缺陷的突变体tango6cq72。在血液细胞中过表达tango6可促使HSPCs扩增。这些结果提示了Tango6具有促进HSPCs扩增和血液发生的生物学功能。进一步研究表明Tango6缺乏导致RNA聚合酶II亚基B(Rpb2)入核受阻且DNA损伤积累,ATM/ATR信号通路显著激活且P53活性增高。P53靶向ikzf1和cmyb并抑制它们的转录,最终导致HSPCs扩增缺陷且血液发生异常。在tango6cq72突变体中回补cmyb和ikzf1可部分恢复永久造血缺陷的表型。
该研究揭示了斑马鱼Tango6-Rbp2信号轴通过ATM/ATR通路来严格调控P53的活性,进而靶向cmyb和ikzf1以有效扩增HSPCs和永久造血。整个研究揭示的Tango6调控HSPCs扩增和血液发生的新机制为有效扩增HSPCs及治疗相关疾病提供新的参考。
参考文献:
1. Orkin, S.H. & Zon, L.I. Hematopoiesis: an evolving paradigm for stem cell biology. Cell132, 631-644 (2008). 2. Mazo, I.B., Massberg, S. & von Andrian, U.H. Hematopoietic stem and progenitor cell trafficking. Trends Immunol32, 493-503 (2011). 3. Wattrus, S.J. & Zon, L.I. Stem cell safe harbor: the hematopoietic stem cell niche in zebrafish. Blood Adv 2, 3063-3069 (2018). 4. Bordignon, C. Stem-cell therapies for blood diseases. Nature441, 1100-1102 (2006). 5. Feng, Z. et al. TANGO6 regulates cell proliferation via COPI vesicle-mediated RPB2 nuclear entry. Nat Commun15, 2371 (2024).
编辑信箱
欢迎您推荐或发布各类关于实验动物行业资讯、研究进展、前沿技术、学术热点、产品宣传与产业资源推广、产业分析内容以及相关评论、专题、采访、约稿等。
我要分享 >热点资讯
- 年
- 月
- 周





