单核苷酸变异(SNVs)是一种与多种疾病相关的遗传变异形式,其中C•G碱基对转变为T•A碱基对的突变几乎占到所有SNVs的50%[1]。CRISPR介导的碱基编辑技术已成为模拟SNVs疾病的一种强大方法,其中胞嘧啶碱基编辑器(CBEs)利用胞嘧啶脱氨酶靶向目标序列并将C•G碱基对转换为T•A碱基对,基于此构建的人类疾病的精准斑马鱼模型为明确临床意义未明的基因突变的致病意义、疾病机制研究和个性化药物筛选提供了绝佳平台[2-4]。然而,现有的斑马鱼CBEs通常具有较宽的编辑窗口,或较强的序列偏好性(偏向于编辑TC和AC基序中的C),或编辑产物不纯、效率仍然较低等缺点,限制了它们在构建人类疾病精准模型中的应用潜力[2,4,5]。2025年02月17日,华南师范大学刘彦梅研究员、广东省人民医院费继锋教授作为共同通讯作者在 Advanced Science 在线发表题为“Sequence Context-Agnostic TadA-Derived Cytosine Base Editors for Genome-Wide Editing in Zebrafish”的研究论文。该研究通过将传统CBE的脱氨酶替换为引入了关键突变的腺嘌呤脱氨酶TadA8e,在斑马鱼中开发了胞嘧啶碱基编辑器工具包zTadA-CBEs。zTadA-BE4max打破了传统的序列偏好,使得GC和CC基序中的C也能被高效编辑,而且比团队之前开发的zevoCDA1-BE4max具有更高的编辑纯度;通过引入SpRY变体产生的zTadA-SpRY-BE4max允许该工具靶向更为广泛的原间隔区相邻基序(PAM);通过调整nSpCas9与TadA的相对位置生成的zTadA-BEmv,与zTadA-BE4max提供了互补的编辑窗口,是首个在斑马鱼中靶向邻近PAM位点的CBE。利用上述工具,作者成功创建了数个此前难以实现的Hermansky-Pudlak综合征、Axenfeld-Rieger综合征精准疾病模型,在F0代同时携带两个致病SNVs的白化病模型,并成功将斑马鱼FMS受体基因突变体fmsts±中的错义突变(T>C)纠正为野生型,恢复其巨噬细胞数量。该工作是刘彦梅团队继前期在斑马鱼中开发了突破PAM限制的碱基编辑器SpRY-CBE4max和zSpRY-ABE8e[4]、高效且低插入/缺失率的ABE-Umax[6]、以及突破了GC、CC限制的zevoCDA1[2]基础上的又一突破。

该研究首先基于前人的研究[7-10],在TadA8e胞嘧啶脱氨酶中引入5个关键突变,N46L/V82S/Q154R/E27H/I49K,替换传统CBE的脱氨酶生成碱基编辑器zTadA-BE4max(图1A)。与斑马鱼碱基编辑器zAncBE4max相比,zTadA-BE4max成功打破了TC的基序偏好,在多个位点展示出高效的GC和CC基序的胞嘧啶编辑,甚至在部分GC和CC位点的编辑效率接近100%(图1B)。此外,从整体上看zTadA-BE4max大幅度提升了编辑效率,在总共测试的25个位点中,仅有3个位点的编辑效率低于10%,相比之下zAncBE4max有17个位点的编辑效率低于10%且相当一部分效率几乎为0%(图1B)。通过对zTadA-BE4max的22个有效编辑位点的进一步分析表明,该工具主编辑窗口在距离PAM远端的4-8位碱基,这与当前主流的碱基编辑器窗口类似[4,5](图1C)。借助zTadA-BE4max,研究人员成功构建了斑马鱼的点突变Hermansky-Pudlak综合征模型(图1D-E),表现出了与人类一致的白化病表型,展示了该工具在构建人类疾病精准斑马鱼模型方面的应用潜力。
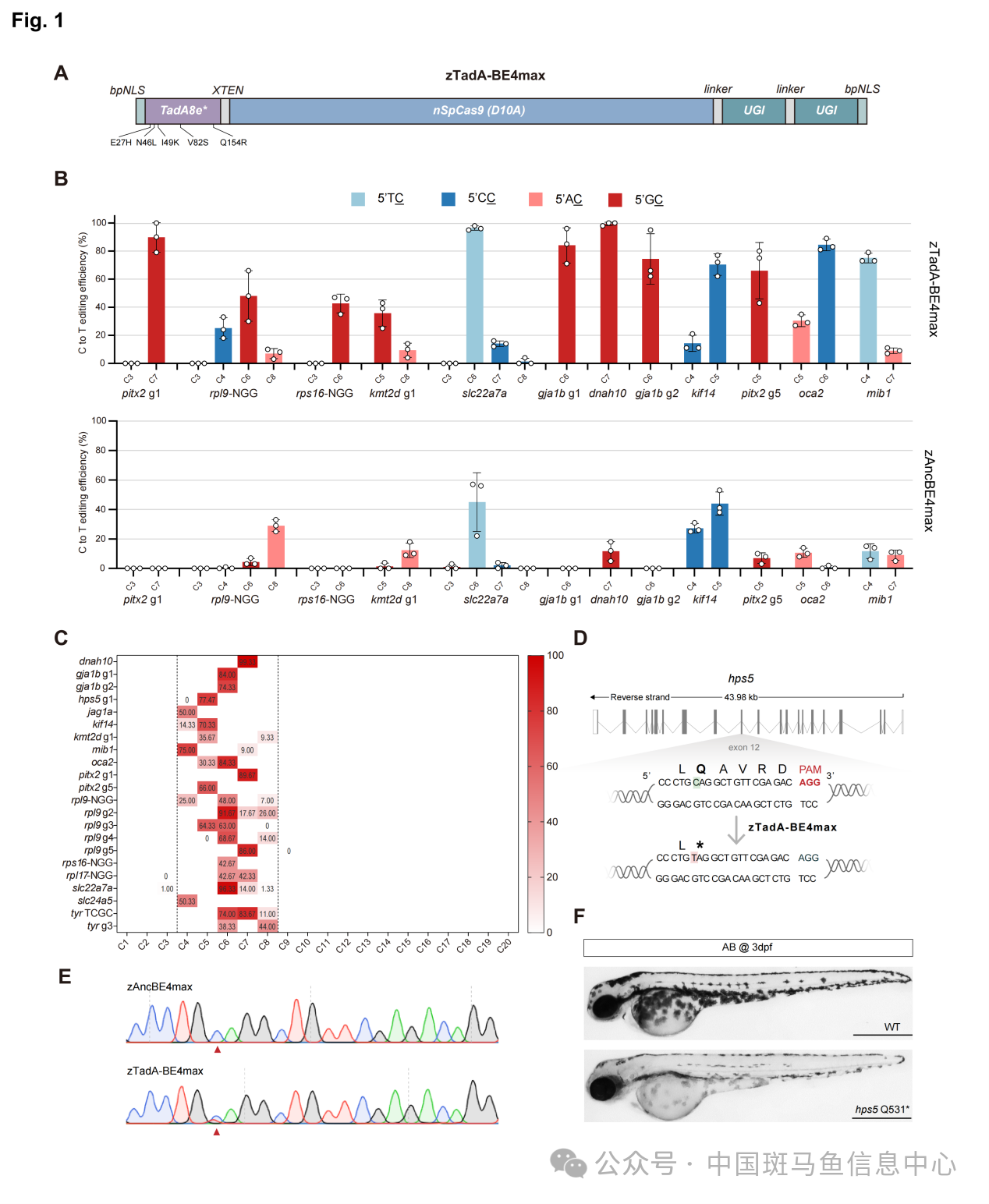
图1 zTadA-BE4max在各序列背景下有效的胞嘧啶基编辑及其构建的精准疾病模型
为了使该工具能够靶向更多的PAM位点,研究人员构建了zTadA-SpRY-BE4max工具(图2A)。与在斑马鱼中主流的无PAM限制工具SpRY-CBE4max相比,zTadA-SpRY-BE4max不仅能够靶向编辑先前难以编辑的GC和CC位点,还大幅度提升了各种基序背景下的胞嘧啶编辑效率(图2B),进一步扩大了碱基编辑器在斑马鱼全基因组的靶向位点。通过对zTadA-SpRY-BE4max的有效编辑位点的进一步分析表明,该工具主编辑窗口在距离PAM远端的4-8位碱基,与团队之前开发的zevoCDA1-198的1-5位 编辑窗口互补(图2C)。利用zTadA-SpRY-BE4max,研究人员成功构建了斑马鱼的点突变Axenfeld-Rieger综合征模型,该模型表现出了与人类患该病时相一致的表型,包括眼部发育异常以及颅面部发育异常等(图2D-G)。该工具的开发为构建更多样的人类疾病精准模型提供可能。
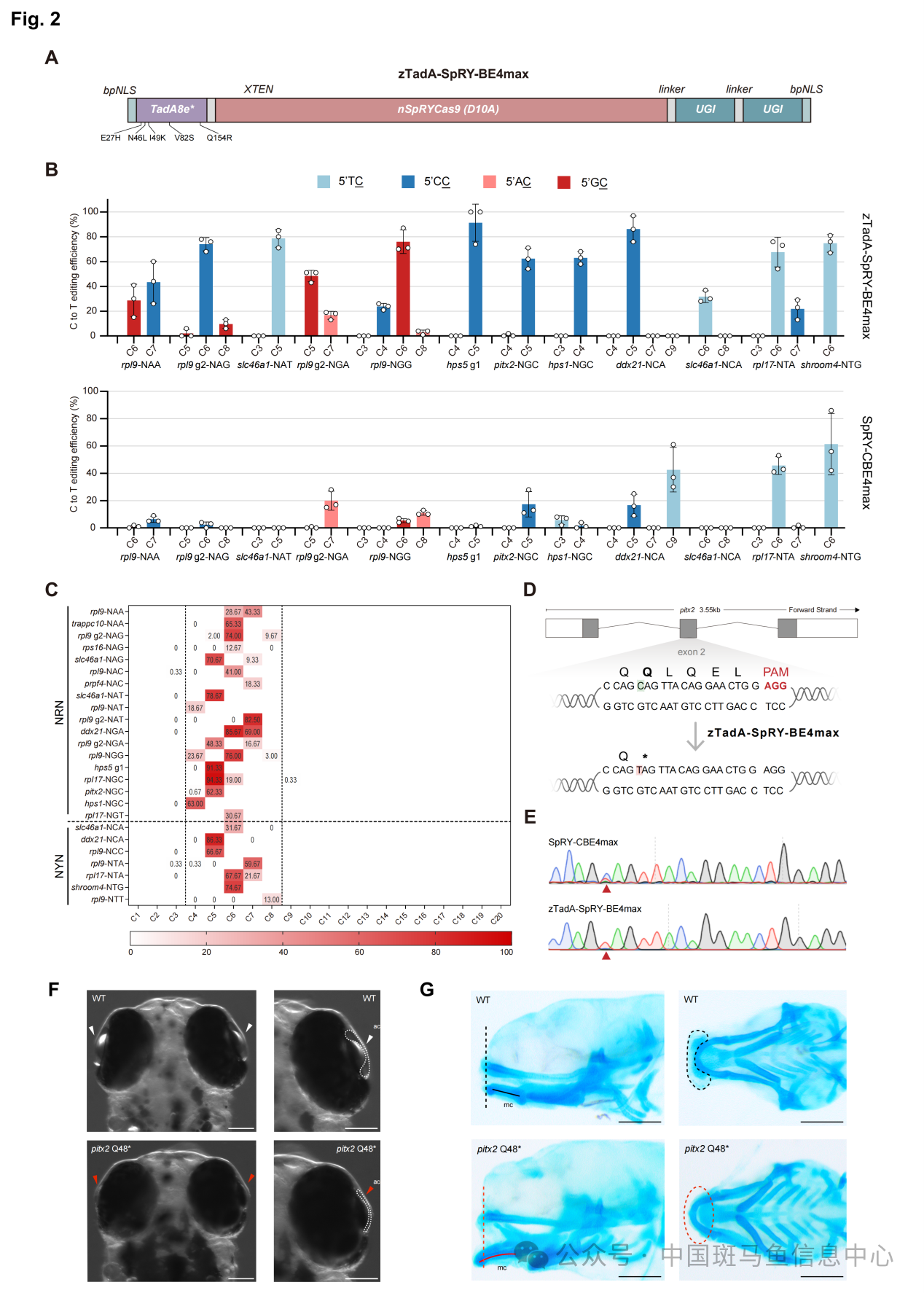
图2 zTadA-SpRY-BE4max在非经典PAM位点的各序列背景中表现出高活性
zTadA-SpRY-BE4max在某些NYN位点仍然无效,这与SpRY本身的偏好性有关[11]。研究人员用TadA脱氨酶二聚体取代了nSpCas9的HNH结构域从而构建了zTadA-BEmv(图3A),在NGG PAM背景下创建了一个互补编辑窗口,其主编辑窗口在距离PAM远端的9-16位碱基(图3C)。zTadA-BEmv表现出了与zTadA-SpRY-BE4max相当的碱基编辑效率(图3B)。利用zTadA-BEmv,研究人员成功构建了另一位点的Hermansky-Pudlak综合征斑马鱼点突变模型,同样表现出了与人类一致的白化病表型(图3D-F)。该工具的出现为弥补了此前窗口的限制,扩大了在斑马鱼中构建人类疾病精准模型的场景。
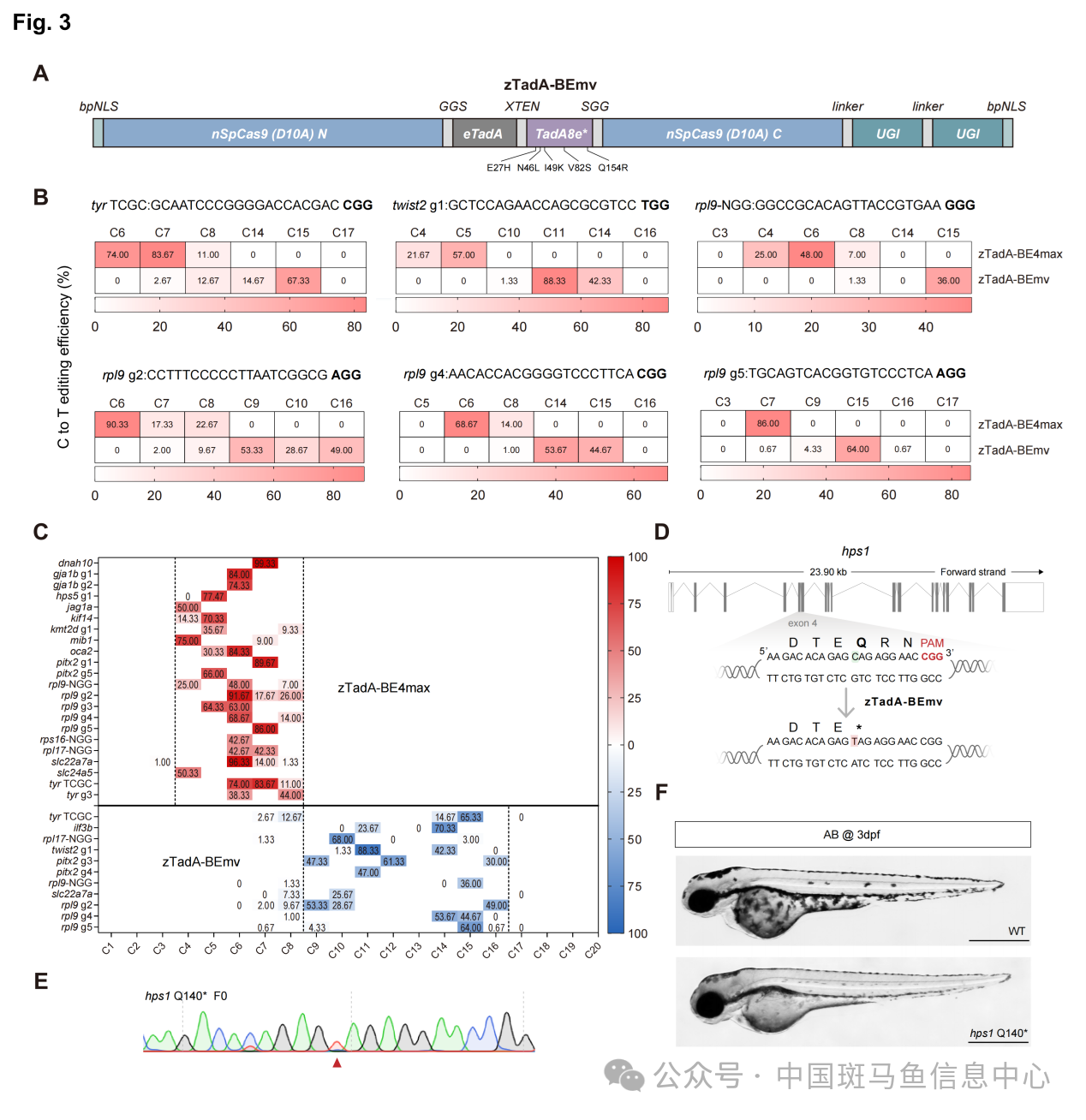
图3 zTadA-BEmv展现出与现有CBEs互补的编辑窗口
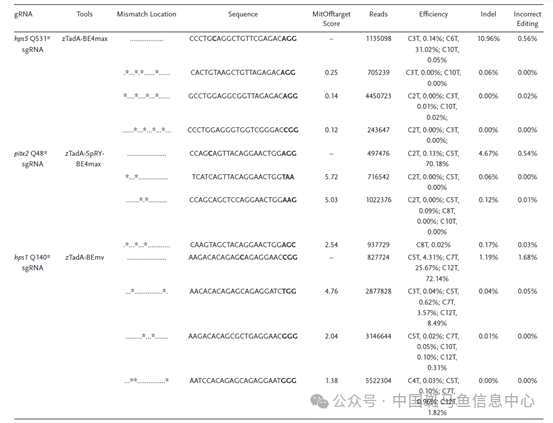
为评估上述工具的脱靶效应以及nSpCas9残留的切割作用的影响,研究人员对上述3个疾病模型进行目标位点和潜在脱靶位点进行高通量测序分析,发现目标位点的插入/缺失(Indel)比例相对较低,分别为(10.96%,4.67%,和1.19%),错误编辑效率同样相对较低(0.56%,0.54%,和1.68%),且测试的潜在脱靶位点的编辑效率都低于10%(大多接近于0),表明利用该工具构建斑马鱼模型分析表型是高效且可靠的。
表1 zTadA-CBEs具有高编辑纯度和低脱靶效应
综上所述,此次研究开发了编辑效率更高、应用场景更广、编辑产物更纯净的新型的胞嘧啶碱基编辑工具包,显著提升了斑马鱼作为研究人类遗传疾病模型的能力,为明确临床意义未明的基因突变的致病意义、探究疾病机制、开发个性化治疗方案提供了更多可能。
华南师范大学脑科学与康复医学研究院已毕业硕士研究生郑少辉、在读硕士生刘洋、夏新欣和肖家旺为该研究论文的共同第一作者。该工作也得到了南方医科大学博士生马惠、华南师范大学硕士生袁萱瑶、张妍、陈子希、博士生彭广聪,以及中国科学院水生生物研究所李文渊老师的协助。作者致谢武汉大学周荣家教授、南方科技大学温子龙教授馈赠质粒和抗体;感谢华南理工大学的徐进教授、陈嘉豪博士,以及中国科学院水生生物研究所的王小四副研究员给予技术支持。该研究得到了国家自然科学基金、国家重点研发计划、广东省人民医院高水平医院建设项目的研究基金支持。
1. Komor, A. C., Kim, Y. B., Packer, M. S., Zuris, J. A. & Liu, D. R. Programmable editing of a target base in genomic DNA without double-stranded DNA cleavage. Nature533, 420–424 (2016).2. Zhang, Y. et al. Cytosine base editors with increased PAM and deaminase motif flexibility for gene editing in zebrafish. Nat. Commun. 15, 9526 (2024).3. Rosello, M., Serafini, M., Concordet, J.-P. & Del Bene, F. Precise mutagenesis in zebrafish using cytosine base editors. Nat. Protoc. 18, 2794–2813 (2023).4. Liang, F. et al. SpG and SpRY variants expand the CRISPR toolbox for genome editing in zebrafish. Nat. Commun. 13, 3421 (2022).5. Zhao, Y., Shang, D., Ying, R., Cheng, H. & Zhou, R. An optimized base editor with efficient C-to-T base editing in zebrafish. BMC Biol. 18, 190 (2020).6. Qin, W. et al. ABE-ultramax for high-efficiency biallelic adenine base editing in zebrafish. Nat. Commun. 15, 5613 (2024).7. Chen, L. et al. Re-engineering the adenine deaminase TadA-8e for efficient and specific CRISPR-based cytosine base editing. Nat. Biotechnol. 41, 663–672 (2023).8. Lam, D. K. et al. Improved cytosine base editors generated from TadA variants. Nat. Biotechnol. 41, 686–697 (2023).9. DNA capture by a CRISPR-Cas9–guided adeninebase editor.10. Gaudelli, N. M. et al. Directed evolution of adenine base editors with increased activity and therapeutic application. Nat. Biotechnol. 38, 892–900 (2020).
11. Walton, R. T., Christie, K. A., Whittaker, M. N. & Kleinstiver, B. P. Unconstrained genome targeting with near-PAMless engineered CRISPR-Cas9 variants. Science 368, 290–296 (2020).










