张文清/刘伟/沈娟合作在斑马鱼实验中揭示c-Myb异常激活和Pu.1缺陷协同促进PHA和sAML发生机制
继发性急性髓系白血病(sAML)是骨髓增生异常综合征(MDS)患者常见的高危进展形式,约30%的MDS患者会在数月至数年内发展为sAML。sAML的发病机制复杂,涉及多种基因突变的累积和相互作用。这表明,AML的发生发展并非由单一基因突变决定,而是多个基因突变以及其相互作用的结果。这些突变共同驱动了造血干/祖细胞的异常增殖、分化障碍及克隆选择,从而导致疾病的发生和进展。其中,c-MYB和PU.1是调控髓系发育的两个重要转录因子,已有的研究表明 c-MYB的过度激活和PU.1的缺陷均与髓系疾病的发生密切相关[1-3],但二者在sAML的进展中是否存在相互作用及潜在的机制尚未明确。
2025年2月28日,华南理工大学张文清教授、刘伟副教授团队联合广东药科大学沈娟教授团队在PNAS上发表题为“ The synergistic effect of c-Myb hyperactivation and Pu.1 deficiency induces Pelger-Huët anomaly and promotes sAML ”的研究论文,揭示了c-Myb异常激活与Pu.1缺陷在sAML发生中的协同作用机制,并提出了新的治疗策略。
c-MYB是调控细胞增殖的关键转录因子,其过度激活常导致细胞增殖失控;而PU.1是调控髓系细胞分化的重要调控因子,其表达不足会导致髓系细胞分化阻滞。该团队前期的研究发现, c-Myb异常激活的斑马鱼c-mybhyper表现为粒细胞大量扩增[4],Pu.1低活性的斑马鱼系pu.1G242D/G242D则表现为髓系前体细胞异常增多[5],且二者均有少部分最终进展为AML。已有研究表明,c-MYB和PU.1的表达在AML中呈负相关[6],但尚不清楚这种表达模式在AML中的意义。此外,Pelger-Huët异常(PHA)是一种以粒细胞核分叶减少为特征的疾病,常与MDS和AML共存,但其与白血病进展的关系尚不明确。
研究团队首先鉴定了一例携带PU.1和c-MYB突变的AML病例,该患者表现出发病早、原始细胞比例高、常规化疗无效等高危特征,同时骨髓血中伴有较高比例的PHA中性粒细胞。通过对在线数据库cBioPortalz中两个独立的AML临床数据进行分析,研究团队发现c-MYB和PU.1的表达呈显著负相关,提示两者在AML进展中可能存在协同作用。
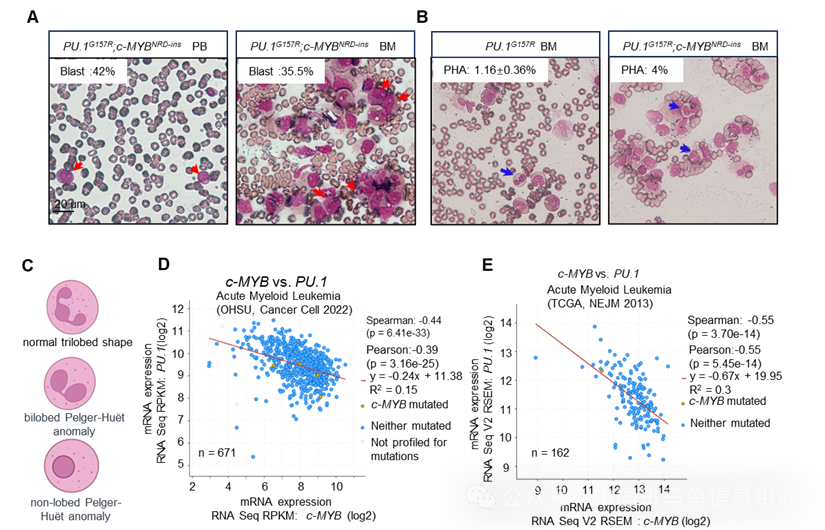
图1 AML患者中的c-MYB和PU.1的异常表达和PHA
进一步研究中,团队利用实验室前期已有的c-Myb过度激活斑马鱼系c-mybhyper和Pu.1缺陷的pu.1G242D/G242D斑马鱼系构建了双变异斑马鱼模型(c-mybhyper; pu.1G242D/G242D),模拟了MDS向sAML的转化过程。结果显示,双变异斑马鱼在胚胎阶段表现出中性粒细胞扩张、发育异常等类MDS特征。有趣的是,成年双变异斑马鱼的肾脏血细胞中出现了高比例(>50%)的PHA样中性粒细胞,其特征为低分叶、核膜不完整、异染色沉积等典型PHA表现(图2A)。通过单细胞转录组测序分析,研究团队发现PHA样中性粒细胞是一组低分化的病态细胞,可能与sAML的转化相关(图2B和C)。

图2 双变异斑马鱼中的类PH细胞是一种病态低分化的中性粒细胞
进一步,研究团队追踪了双变异斑马鱼的生存和AML转化情况。结果显示10月龄双变异斑马鱼 的生存率显著降低,相较于单基因变异斑马鱼,双变异斑马鱼AML的发病率显著上升,高达36%(图3)。
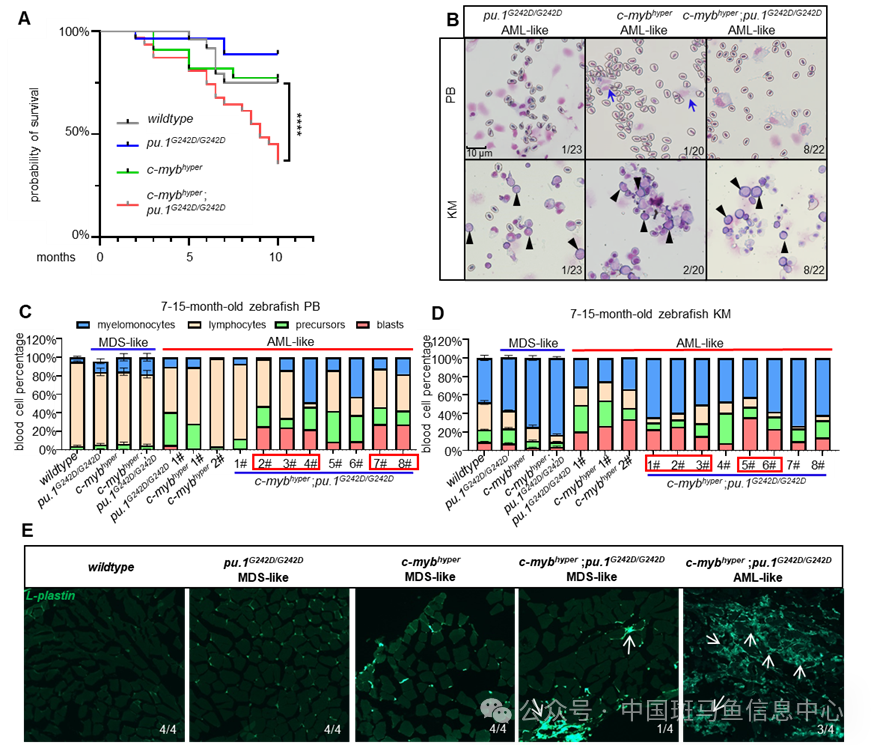
图3 双变异斑马鱼具有高死亡率和高sAML转化率
已有的研究表明,原发PHA由LBR基因的异常所致。此外,近年研究提示,在造血干/祖细胞(HSPC)中敲低LMNB1(LBR的配体基因)的表达,可导致PHA样细胞的产生以及髓系分化倾向[7]。基于这些背景,研究团队首先检测了双变异斑马鱼模型中lmnb1的表达水平,并发现其显著降低。为进一步验证lmnb1在PHA和MDS/sAML进展中的作用,研究团队进行了正反向遗传验证实验。在野生型斑马鱼中敲低lmnb1表达,导致PHA样细胞和原始细胞数量显著增加;而在双变异斑马鱼中过表达lmnb1,则部分挽救了PHA表型。这些结果表明,c-Myb的过度激活和Pu.1的缺陷能够协同降低lmnb1的表达,从而诱导PHA样中性粒细胞的发育,并促进MDS向sAML的进展。

图4 lmnb1缺失导致斑马鱼类PHA和AML表型
在此双变异斑马鱼模型的基础上,研究团队还发现,细胞周期抑制剂阿糖胞苷(Ara-C)和分化诱导剂全反式维甲酸(ATRA)的联合用药可以有效缓解双变异斑马鱼的AML和PHA症状(图5)。这一发现为sAML的治疗提供了新的策略,提示Ara-C和ATRA的联合用药方案有望成为携带PU.1和c-MYB双变异、del5q(含LMNB1缺失)以及高PHA水平的AML患者的一种新的治疗选择。
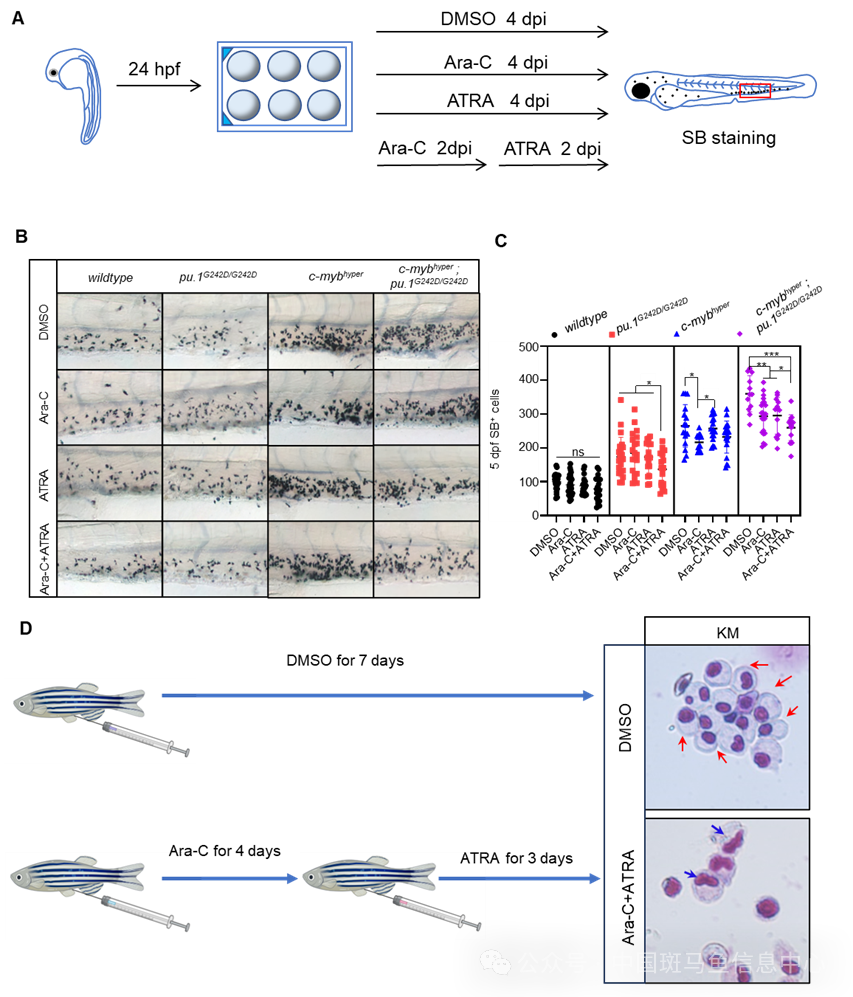
图5 Ara-C和ATRA联合用药的治疗效果
该研究揭示了c-Myb异常激活和Pu.1缺陷通过协同降低lmnb1表达诱导PHA并促进MDS/sAML转化的机制。c-mybhyper; pu.1G242D/G242D 斑马鱼模型可作为有效的sAML模型用于药物筛选,为相关AML患者提供了新的治疗思路(图6)。
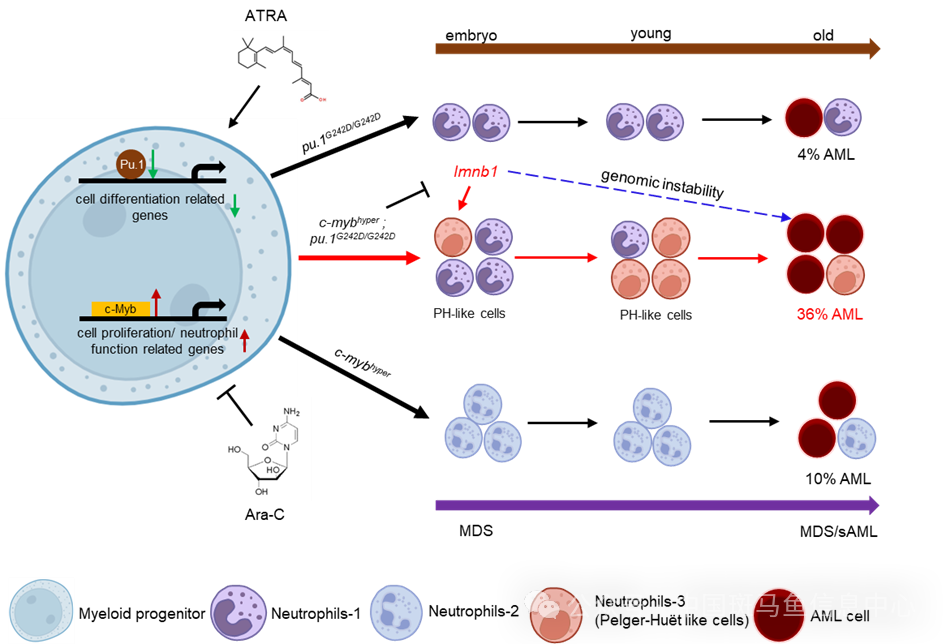
图6 c-Myb和Pu.1协同促进sAML发生的模型
华南理工大学徐颂恩博士、洪佳馨硕士为该论文共同第一作者,南方医科大学南方医院薛容涛博士为该研究的血液表型鉴定部分作出了重要贡献。华南理工大学刘伟副教授、张文清教授,以及广东药科大学沈娟教授为该论文的共同通讯作者。本研究受到国家自然科学基金、国家重点研发计划等项目的支持。
1. A. Tomita et al., Truncated c-Myb expression in the human leukemia cell line TK-6. Leukemia 12, 1422-1429 (1998).
2. E. Clappier et al., The C-MYB locus is involved in chromosomal translocation and genomic duplications in human T-cell acute leukemia (T-ALL), the translocation defining a new T-ALL subtype in very young children. Blood 110, 1251-1261 (2007).
3. F. Rosenbauer et al., Acute myeloid leukemia induced by graded reduction of a lineage-specific transcription factor, PU.1. Nat Genet 36, 624-630 (2004).
4. W. Liu et al., c-myb hyperactivity leads to myeloid and lymphoid malignancies in zebrafish. Leukemia 31, 222-233 (2017).
5. J. Sun et al., Suppression of Pu.1 function results in expanded myelopoiesis in zebrafish. Leukemia 27, 1913-1917 (2013).
6. P. Basova et al., Aggressive acute myeloid leukemia in PU.1/p53 double-mutant mice. Oncogene33, 4735-4745 (2014).
7. A. Reilly et al., Lamin B1 deletion in myeloid neoplasms causes nuclear anomaly and altered hematopoietic stem cell function. Cell Stem Cell 29, 577-592 e578 (2022).
编辑信箱
欢迎您推荐或发布各类关于实验动物行业资讯、研究进展、前沿技术、学术热点、产品宣传与产业资源推广、产业分析内容以及相关评论、专题、采访、约稿等。
我要分享 >热点资讯
- 年
- 月
- 周





