王璐团队在斑马鱼研究中发现转录因子Jund动态协调顺式调控元件促进内皮造血转化
在发育过程中,基因时空表达的精确调控是细胞命运决定的关键,该过程主要依赖于顺式调控元件(cis-regulatory elements,CREs)与转录因子的动态互作。其中,广泛表达的转录因子维持发育的基本程序,谱系特异转录因子则进一步指导特定类型细胞的命运选择和功能实现[1]。然而,不同类型的转录因子如何通过协同互作,动态结合顺式调控元件并调控其活性的分子机制,仍有待阐明。
造血干/祖细胞(hematopoietic stem and progenitor cells,HSPCs)由一群具有生血潜能的内皮细胞,即生血内皮细胞,通过内皮造血转化(endothelial-to-hematopoietic transition,EHT)过程产生[2]。在此过程中,内皮相关顺式调控元件逐渐失活,而造血相关顺式调控元件被激活[3]。这些“分子开关”通过协调基因的时序性表达,驱动造血干/祖细胞的生成。但是,顺式调控元件与转录因子如何动态协作,促进细胞命运的有序转变,仍是未解之谜。
2025年6月初,中国医学科学院血液病医院(血液学研究所)王璐团队在PNAS发表题为 “Jund orchestrates cis-regulatory element dynamics to facilitate endothelial-to-hematopoietic transition” 的文章,揭示了内皮造血转化过程中顺式调控元件重塑与转录因子结合的动态变化规律,发现转录因子Jund与Hoxa9a协同作用抑制生血内皮细胞的内皮特性,促进其造血命运的获得。

研究人员首先分析了斑马鱼顺式调控元件相关组蛋白修饰(H3K4me3、H3K27ac和H3K27me3)景观,发现增强子和启动子的协同激活是内皮-造血转化的基础。其中,相邻发育阶段共享的过渡型增强子可预先激活后续发育所需基因,而内皮细胞、生血内皮细胞与造血干/祖细胞特异性增强子则分别调控其对应细胞的特征性基因程序。转录因子基序富集和共定位分析显示,转录因子AP-1与谱系特异转录因子共同结合于细胞类型特异的增强子位置,并形成时空动态组合,介导增强子的阶段性激活。功能缺失与回救实验证实,AP-1家族成员Jund以内皮细胞自主性方式促进造血干/祖细胞产生。机制研究显示,Jund与Hoxa9a结合于内皮发育关键基因dll4增强子区域,引起H3K27ac修饰水平下调,降低 dll4转录活性,从而有效关闭内皮特性维持程序,最终促进生血内皮细胞向造血命运的转变。
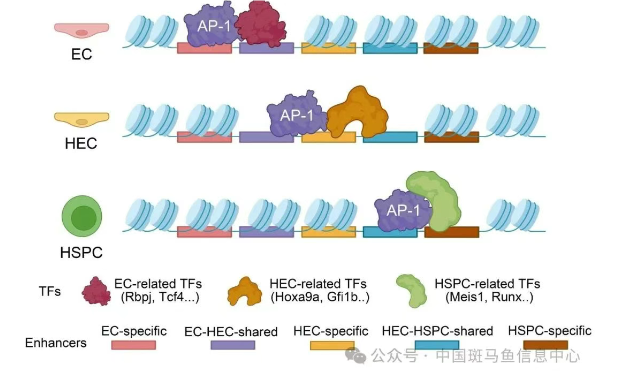
图1. 内皮造血转化过程中转录因子AP-1的作用模式图
综上所述,该研究揭示了内皮造血转化过程中转录因子AP-1的关键调控作用(图1),阐明了其成员Jund与Hoxa9a协同促进生血内皮细胞命运决定的分子机制,为理解造血干细胞发育的表观遗传调控提供了新视角。
中国医学科学院血液病医院(血液学研究所)博士生郭佳妮、科研助理刘梦瑶为共同第一作者,王璐研究员为通讯作者。感谢刘峰研究员的帮助和支持。该研究得到了国家自然科学基金、天津市杰出青年基金以及中国医学科学院创新工程项目资助。
参考文献
1.Li, F., et al., ERG orchestrates chromatin interactions to drive prostate cell fate reprogramming. J Clin Invest, 2020. 130(11): p. 5924-5941.
2.Bertrand, J.Y., et al., Haematopoietic stem cells derive directly from aortic endothelium during development. Nature, 2010. 464(7285): p. 108-11.
3.Gao, P., et al., Transcriptional regulatory network controlling the ontogeny of hematopoietic stem cells. Genes Dev, 2020. 34(13-14): p. 950-964.
编辑信箱
欢迎您推荐或发布各类关于实验动物行业资讯、研究进展、前沿技术、学术热点、产品宣传与产业资源推广、产业分析内容以及相关评论、专题、采访、约稿等。
我要分享 >热点资讯
- 年
- 月
- 周





