犬腺病毒感染与实验犬质量控制
犬腺病毒(Canine adenovirus, CAV)以血清型为划分标准,包括犬腺病毒Ⅰ型(Canine adenovirus 1, CAV-1)和犬腺病毒Ⅱ型(Canine adenovirus 2, CAV-2)。具体而言,CAV-1主要导致犬类罹患严重的急性败血性肝炎,该病发病急骤,病情凶险,对犬类的健康构成极大威胁。此外,CAV-1的感染范围不仅限于犬类,它还可能跨越物种界限,引发熊和狐狸等野生动物的脑炎,对这些动物的神经系统造成损害。而CAV-2则主要造成犬科动物患上传染性喉气管炎,该病以呼吸道症状为主,包括咳嗽、喉部肿胀等,严重时可能影响犬的呼吸功能。同时,CAV-2还可能引起传染性腹泻,对犬科动物的消化系统造成不良影响。CAV作为双股DNA病毒,属于哺乳动物腺病毒属,致病性强。CAV对犬养殖业及相关毛皮经济动物养殖业造成了经济损失,同时严重威胁着动物的健康,因此吸引了全球众多研究学者的密切关注。
一、病 原
分类地位:
犬腺病毒(Canine Adenovirus,CAV)是腺病毒科中哺乳动物腺病毒属的一员。腺病毒科是一个庞大的病毒家族,已经被确认超过44种病毒,其宿主范围广泛,各不相同。当前,测序技术以其高效且低成本的特点,为病毒研究提供了有力支持,预示着未来有望不断发现新的腺病毒属种,甚至可能揭示全新的病毒物种。Green等[1]于1925年首次从狐狸中发现CAV-1; Dithfield等[2] 于1962年从犬中成功分离出了CAV病毒。这个毒株开始被认为是CAV-1的弱毒株,但后续的研究被确认为CAV-2[3-7]。CAV-1与CAV-2均归类于腺病毒科下的哺乳动物腺病毒属,它们在抗原特性和基因组成方面具有紧密联系。具体而言,这两种病毒在核苷酸序列上的同源性高达75%,这一数据进一步证实了它们之间的密切亲缘关系[8, 9][8, 9][8, 9],CAV-1与CAV-2在血凝特性及病毒对特定组织的亲和力方面展现出了显著的差异。具体来说,这两种病毒都能凝集人类“O”型红细胞以及白化病毒大鼠红细胞,但它们在凝集效率、所需条件以及凝集后的形态变化等方面可能存在不同。CAV-1能够特异性凝集豚鼠和鸡的红细胞,CAV-2则无法凝集[10]。CAV-1病毒主要在血管内皮细胞中活跃增殖,并深入肝、肾等器官的实质细胞内进行复制与扩散,直接损害机体的循环系统和内脏器官。而CAV-2则更倾向于在呼吸道上皮和肠上皮内进行复制,影响呼吸系统和消化系统的正常功能[6, 11, 12][11]。
形态学基本特征:
CAV具有线状双链DNA基因组,无囊膜、呈二十面体立体对称。基因组长约30~31 kb,以线状形式盘曲于病毒衣壳内部。根据基因转录时间的差异,CAV的基因组可以被细分为多个区域,包括E1A、E1B、E2A、E2B、E3、E4以及L1至L5区等。这些区域分别编码病毒的关键结构蛋白,如纤维蛋白、五邻体蛋白、六邻体蛋白以及衣壳蛋白等,这些结构蛋白共同构成了病毒的完整形态。犬腺病毒的E1区是病毒复制需的关键区域,一旦发生缺失,重组后的CAV载体会失去自主复制增殖能力,只能依赖特殊的工程细胞或非缺失的腺病毒完成自我增殖。另外,若是在E3区插入外源基因构建CAV载体,得到的载体为复制非依赖型。它能够在体内自主复制,并表达所插入外源基因编辑的蛋白。因此,这类载体在诊断抗原的制备、蛋白特性研究以及载体疫苗的开发等多个领域,均得到了广泛的应用[13]。
理化特性:AV展现出较强的抵抗力,能够耐受热、干燥等严苛环境条件,并且对乙醚、胆酸盐、氯仿等多种脂溶性溶剂均不表现出敏感性。在4℃的低温环境下,CAV能够存活6~9个月之久;即便在-20℃的极寒条件下,它也能保持活性并长期存活。然而,当环境温度升高至56℃时,CAV的活性会被破坏。但在极端寒冷的条件下, CAV能够存活时间有所延长,约200天。此外,CAV在pH值为2~5的范围内表现稳定,但在pH值低于2或高于10的极端酸碱环境中则变得不稳定。尽管如此,CAV仍能酸碱度适宜在胃肠道中保持其活性。
分子生物学:
CAV-1的核酸结构是一种线状双链DNA分子,其基因组全长测定约为31 kb。CAV-2的基因组全长约为32.2 kb左右。尽管CAV-1和CAV-2在核酸序列上存在一定的相似性,它们的同源性大约为70%左右,但在基因水平上,两者的相关性却相对较低,仅约为56.6%。进一步分析CAV-1的基因组结构,可以将其细分为E1-E4和L1-L5等多个区域。在这些区域中,E1和E2尤为关键,它们各自又可以进一步划分为A和B两个子区域。这些区域共同编码了多达15种不同的多肽,这些多肽在病毒的结构和功能中发挥着重要作用。其中,结构性蛋白占总蛋白量90%以上的最主要包括五邻体蛋白、六邻体蛋白、纤突蛋白以及核衣壳蛋白等,这些蛋白共同维持病毒的稳定结构和感染能力。
五邻体结构分为基底和纤突,基底位于腺病毒二十面体的顶角。纤突通过非共价键与基底连接,并且关乎腺病毒的抗原特异性。六邻体携带有能引发补体结合反应的抗原,而五邻体是完全可溶于水的血凝素。腺病毒序列较保守,但最近有发现CAV-1毒株在pV Ⅲ基因序列与CAV-2有所变异。
CAV-2基因组属于线性基因,病毒无囊膜,衣壳由252个壳粒组成,这些壳粒排列成二十面体对称结构。其中,240个壳粒为六邻体,位于病毒粒子的主要部分;另外12个壳粒为五邻体,位于病毒粒子的顶点位置。五邻体上有突出的纤丝,这些纤丝是病毒粒子的重要特征之一。另一方面,六邻体蛋白不仅在腺病毒中占据数量上的优势,而且是其衣壳中体积最为庞大的结构蛋白。这些六邻体由三个结构相同且功能协同的多肽亚单位紧密组合而成,它们进一步细分为形态鲜明的顶部区域和稳固的基底部。而这些精心构建的六邻体蛋白,作为关键的结构组件,又共同协作、精密排列,从而构成了腺病毒粒子外层那复杂而坚固的衣壳结构,为病毒提供了必要的保护与稳定性。衣壳顶部呈现出三角形,而基底部状似六边形,彼此之间紧密相连,但与五邻体的连接较为疏松。在腺病毒的二十面体结构的每个平面中心,既围绕着9个六邻体,又巧妙地分布着构成病毒关键角色——12个拷贝的蛋白IX。然而,研究者在腺病毒属的其他四个亚类中并未发现蛋白IX,这一发现进一步揭示了腺病毒不同亚类之间在结构组成上的差异。
培养特性:CAV-1可以在多种细胞系中进行培养,包括MDCK(Madin-Darby Canine Kidney)细胞,猪和水貂的肺细胞和肾细胞等。其中MDCK细胞是CAV-1最易感染的细胞类型。相比之下,CAV-2的感染范围较为局限,主要限于犬细胞,对其他种类的动物细胞则不太敏感。CAV-1在感染宿主细胞后,会在细胞内形成包涵体。包涵体的形成是病毒感染细胞的一个重要标志,也是病毒复制和增殖的结果。当CAV-1病毒侵入并感染细胞后,它会遵循一个特定的生物学过程来释放病毒粒子。这个过程包括核膜的退行性变化,这种变化为病毒粒子的释放创造了有利条件,使得它们能够顺利地从被感染的细胞中逸出,进而继续感染其他健康细胞。而CAV-2则采用不同的机制,即通过出芽的方式从感染细胞的表面释放病毒粒子。值得注意的是,CAV-1在细胞上进行连续多代的培养后,其毒力往往会有所减弱,即出现致弱现象。CAV-2可以在犬类和猪类的肾原代及传代细胞系上生长,并引起相关细胞发生典型的细胞病变。
为了培养和驯化犬腺病毒Ⅱ型毒株,研究人员使用了MDCK细胞成功分离出了CAV-2-SY-5毒株[14]。经过传代和驯化,CAV-2-SY-5可以突变为CAV-2弱毒株。此外,夏咸柱从幼龄病犬中分离出了CAV-2毒株——YCA18。另外还有实验进一步验证了CAV-2的致病能力和细胞感染特性,接种DK细胞系(Dog Kidney,DK)与PK细胞系(Porcine Kidney,PK)的实验结果显示两种细胞均出现了明显的细胞病变。 CAV2-XN3毒株在MDCK细胞培养时增殖迅速且稳定,并且能够有效地诱导细胞产生明显的病变效应,表现出强烈的致病性和感染性。然而在其他类型的细胞上,并未观察到类似的病变情况。Ashwini Ramidi等科研人员使用MDCK细胞分离出6株CAV-2毒株,并且这些CAV-2毒株与美洲和欧洲的毒株在遗传关系上紧密相关[15]。
二、流行病学
CAV-1和CAV-2这两种病毒都可以在感染或康复犬的粪便和尿液中找到,因此,这些排泄物成为对健康犬构成感染威胁的主要源头。CAV-2的感染范围比CAV-1更为狭窄,主要感染犬科动物,引发上呼吸道和消化系统疾病。发病动物和康复后的病毒携带者是CAV的主要传播源。此外,携带病毒的犬只也可能通过胎内传播导致幼犬患病甚至死亡。对于已经康复的动物,其尿液中仍可能携带病毒长达6个月之久,这意味着CAV也能通过非直接接触的方式传播。Andrea Balbon等科研人员在蝙蝠体内检测到了CAV的存在,他们发现,部分腺病毒毒株与CAV存在紧密的遗传联系,这一发现揭示了蝙蝠与哺乳动物食肉动物之间可能存在病毒跨物种传播的情况。这一研究成果进一步明确了野生食肉动物在CAV流行病学中作为中间宿主的重要角色。
CAV-2主要感染犬和狐狸、貉、狼等野生犬科动物。一般来说,野生动物感染后没有典型的临床表现,但在解剖后会发现有轻微的病理变化。兔子、刺猬、松鼠、马和猩猩也是CAV的中间宿主。对大熊猫进行的CAV抗体研究发现,CAV也可感染熊。CAV-2感染犬一般为良性经过,感染10-14天后逐渐康复。CAV-2病毒感染常见于4月龄以内的幼犬,因其可导致犬群集体咳嗽,故又称“犬窝咳嗽”。
三、临床症状
1.CAV-1感染:CAV根据感染条件不同潜伏期有所差异,犬在自然条件和人工实验条件下感染后的潜伏期分别为6~9天和2~6天。CPV感染后根据临床症状表现可分为三种类型,在最初感染时表现为最急性型,因死前无明显的症状表现不能及时治疗,感染犬可立即死亡。急性型的初步症状为体温升高(高于40 ℃),其次表现出精神、食欲状态下滑,并伴有呕吐、眼鼻溢物等,病情严重者一周内死亡。慢性型病例多发生在感染后期,患病犬体温升高不明显,食欲异常,可能伴有胃肠反应,几乎无死亡病例,但是生长发育会在一定程度上受损,且有可能长期排毒[16]。流涎、共济失调等神经症状在患犬中很少见,但是会引起中枢神经系统血 管损伤[17, 18]。
2.CAV-2感染:CAV-2感染造成犬传染性喉气管炎的病例,潜伏期为5~6天,潜伏期后患犬体温持续性升高(部分犬体温超过40℃),随后出现喷嚏、干咳或湿咳、精神不振和沉郁、胃肠道异常反应、呼吸困难、鼻眼有异物分泌等[19]。CAV-2与其他病原造成混合感染,引起“犬窝咳”。
四、病理变化
大体解剖观察:
1.CAV-1剖解变化:肝脏肿胀:肝脏可能呈现肿胀状态,质地变脆,边缘变钝。肝小叶变化:肝小叶结构可能变得明显,切面外翻。胆囊变化:胆囊壁可能出现明显的水肿和增厚,有时伴有出血点,整个胆囊可能呈黑色,胆囊粘膜有纤维蛋白沉着。其他变化:腹腔内常有积液,液体清朗且常含血液和纤维蛋白,暴露空气后极易凝固。此外,胃肠道可能出血,肾充血,肠系膜淋巴结肿大、出血。偶有患犬肺脏局部肺泡隔增宽,其内血管淤血、出血等[20]。
2.CAV-2剖解变化:CAV-2剖检变化主要有支气管淋巴结变化:支气管淋巴结和肠系膜淋巴结可能出现明显的充血。肺炎变化:肺部可能出现严重的肺炎病变。肺脏膨胀不全、充血,发生大面积实变;喉头出现出血点或有黏液[20]。组织病理学观察可见坏死性支气管肺炎,肺泡II型上皮细胞增生,肺泡隔增宽,肺泡腔内有大量脱落细胞、巨噬细胞等细胞性渗出物,且上皮细胞和肺泡巨噬细胞内出现核内包涵体等[21]。
组织病理学观察:常见的特征包括:肠道病变:感染犬腺病毒后,肠道会出现明显的病变,包括充血、水肿、糜烂和溃疡。特别是小肠黏膜上皮细胞的变性、坏死和脱落。淋巴组织受损:犬腺病毒会侵害淋巴组织,尤其是肠管和相关的淋巴组织。细胞病变:犬腺病毒感染引起的细胞病变主要包括上皮细胞的变性、坏死和脱落。综上所述,犬腺病毒感染的组织病理学观察主要呈现为肠道病变、淋巴组织受损和细胞病变。
五、诊断
1. CAV-1
通常,依据流行病学特征、临床表现以及解剖病理学检查(含包涵体检测)的结果,可对该病进行初步诊断。值得注意的是,该病的肝炎型初期症状与犬瘟热、钩端螺旋体病等存在相似性,且存在并发感染的可能性,因此鉴别诊断至关重要,具体鉴别要点可参考犬瘟热的诊断方法。对于这两种病型的最终确诊,方法相同,均依赖于病毒的分离、鉴定以及血清学检测。
病毒分离步骤包括:在活体动物发热初期采集血液、扁桃体拭子及尿液样本,对于死亡动物则采集肝脏、脾脏等组织样本。经过适当处理后,这些样本被接种到犬肾原代及传代细胞、易感幼犬或仔狐的眼前房中。接种后,腺病毒的特征性细胞病变通常在30小时至6至7天内显现,同时可检测到包涵体的存在;在后者(指易感幼犬或仔狐)中,可能出现角膜混浊并产生包涵体。血清学检测方面,通过荧光抗体检查扁桃体涂片可提供疾病的早期诊断。同时,采集发病初期及之后14天的两份血清样本进行凝集抑制试验,若抗体滴度升高4倍或以上,则可作为当前感染的证据。此外,补体结合试验、琼脂扩散试验、中和试验以及皮内变态反应等方法同样可用于疾病的诊断。
国外已经研发出多种分子诊断技术,其中一种方法是通过选取病毒早期转录区中的保守序列作为引物,建立了PCR检测技术。这项技术有望应用于本病的临床诊断和治疗中。
2. CAV-2
近年来,分子诊断技术取得了显著进展,为临床快速、准确检测病原体提供了巨大技术支持。对于临床疑似CAV-2病毒感染犬,首先观察其是否表现出上呼吸道和消化系统症状,并结合流行病学调查、临床症状分析及病理学检查,可做出初步诊断。进一步确诊则需通过实验室诊断,目前通过实验室技术诊断CAV-2的方法包括PCR、实时荧光定量PCR、病毒分离、电镜观察、血清学诊断等。
实验室对病毒的分离鉴定常采用细胞分离技术,过观察细胞病变来确认结果利用MDCK细胞分离CAV-2病毒已成为实验室的常规操作。如范泉水等人利用MDCK细胞成功分离出CAV-2毒株SY株,并观察到MDCK细胞呈现葡萄串状病变。夏咸柱等人则从一只幼龄病犬中分离出CAV-2毒株,命名为YCA18,该毒株在MDCK细胞上同样表现出通透性增强、体积变大变圆、聚集成葡萄串状等典型病变,而F81、Vero、BHK-21、CEF细胞则无此病变。
随着现代科技的飞速发展,犬腺病毒的分子生物学技术取得了显著进步,为CAV-1和CAV-2的鉴别提供了坚实的生物技术支撑。姚大伟等研究者通过对比PCR产物及限制性内切酶切位点的特性,成功区分了CAV-1与CAV-2两种病毒。他们发现,相较于直接对病料样本进行PCR检测,先通过细胞分离病毒后再执行PCR检测的方法能够提供更高的准确性。尽管如此,出于提升检测速度与效率的目的,常规PCR技术依然被广泛用于直接检测病料样本,这在宠物医院中尤为关键,有助于实现病料的快速检测与个性化治疗方案的制定。因此,对于临床初步诊断而言,直接利用PCR技术对临床病料进行检测被视作一种更为适宜的方法。另外,Uttara Chaturvedi等人还开发了一种针对粪便或尿液样本中犬腺病毒的PCR检测方法,该方法通过有效消除样本中的抑制成分,显著增强了PCR检测法在CAV临床检测中的适用性和准确性。
采用CAV荧光抗体技术,结合心、肝、脾、肺、肾等组织切片及印片,以及感染培养物中的CAV抗原,能够进一步提升诊断的准确性。过往对CAV的研究主要依赖于血清学方法,而病毒分离技术的应用则相对较少。值得注意的是,CAV-1与CAV-2之间存在交叉反应。然而,常用的血清学方法无法有效区分CAV-1和CAV-2,仅有血凝抑制试验能够实现对这两种CAV类型的区分。
SYBR Green实时PCR测定结合熔解曲线分析,能够高效且特异性地鉴别CAV-1和CAV-2,展现出高灵敏度和良好的可重复性。Giulia Dowgier等人开发了一种创新的双重实时荧光PCR方法,该方法采用单一引物和病毒特异性探针,能够同时检测和鉴定CAV-1与CAV-2。该方法可广泛用于实验室确认犬腺病毒感染,并为家犬及野生食肉动物种群的流行病学研究提供快速准确的结果。
经过磷钨酸负染以及戊二醛与俄酸的双重固定步骤后,在电子显微镜下,CAV-2病毒粒子展现出了清晰的二十面体对称结构,其直径大约为80纳米。病毒粒子的核衣壳外层排列着整齐有序的壳粒。此外,在细胞核内部,可以观察到腺病毒粒子以晶格形式排列,以及它们的前体形态。这些电子显微镜下的观察结果不仅描绘了CAV-2的形态特征,还为病毒的提纯流程以及全病毒抗原的制备工作提供了有益的参考依据。
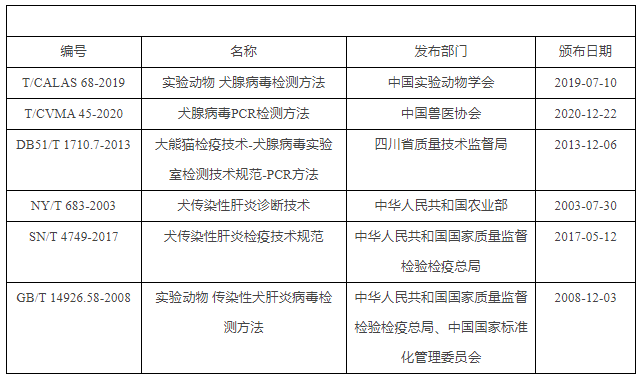
检测标准:
六 防治措施
1. CAV-1
研究发现, CAV-1疫苗对CAV-2不能产生完全保护,但CAV-2疫苗可以使之产生CAV-1的抵抗力,故常用CAV-2弱毒苗免疫犬抗CAV-1感染。
目前,治疗犬传染性肝炎的主要手段包括特异性疗法、抗病毒疗法和输液疗法等。在治疗方面,可采取肌肉注射或皮下注射方式给药。对于可能受到感染或易感犬类,建议使用犬传染性肝炎的高免血清进行预防性注射。抗病毒治疗是对患有犬传染性肝炎的动物使用含有病毒成分的制剂或液体来预防和控制疾病的传播。抗病毒疗法的核心步骤是向犬类注入干扰素,并根据它们的体型差异来选择适当的剂量。治疗方法是肌肉注射,每天进行两次注射,整个治疗周期为5~7天。免疫调节疗法是针对病毒引起的疾病而设计出来的一种治疗手段,一般采取静脉注射的形式。在进行抗病毒治疗的过程中,也可以选择口服抗病毒药物来达到治疗效果。同时,还应该加强护理措施,保证犬能够安全度过发病阶段。
CAV-2
为了预防CAV-2,最有效的方法是进行免疫预防。最初,我们使用CAV-1的灭活毒株进行预防,但随着免疫用量的增加和免疫期的缩短,我们最终选择使用CAV-1细胞来培养弱毒苗。通过MDCK细胞传代的弱毒,再通过猪肾细胞的连续传代,可以有效地避免弱毒的返祖现象,其中病毒疫苗和抗乙型肝炎表面抗原抗体联合使用为首选,同时还可以采取其他一些措施辅助治疗。由于CAV-1和CAV-2之间存在交叉保护机制,CAV-2能够为CAV-1提供全面的保护。但是CAV-1无法有效预防CAV-2导致的传染性喉气管炎等相关症状。因此,目前普遍使用CAV-2来预防CAV-1和CAV-2的发生。如果犬群中出现了某种或多种病原体同时存在,那么就需要考虑使用多联疫苗联合接种方式进行预防。对那些刚被感染或可能被病毒感染的狗进行高免血清注射,能够实现紧急的预防和治疗效果。
当犬被CAV-2感染并患上传染性喉气管炎时,首要任务是进行抗菌和消炎处理,以增强其对疾病的抵抗能力,如果出现呼吸困难,咳嗽等症状,应及时就诊并做相应处理。在疾病进展迅速的情况下,通常可以为患病的犬只注入高免血清以进行急救。如果犬群中有患有严重肺炎或者是病毒性肠炎的患犬出现这种症状后,则需要在短时间内采取积极有效的措施进行救治。也可以采用抗病毒药物进行对症疗法。同时应加强饲养管理,提高犬体免疫力,避免继发其他疾病。
七 犬腺病毒感染对实验犬及动物实验的影响
犬感染CAV的情况极为普遍。据研究,美国有82%的幼犬血清中检出CAV中和抗体阳性。在20世纪初期,Green和 Dewey等人首次发现犬腺病毒Ⅰ型(CAV-1)。而CAV-2则于1962年由Ditfield等人从犬的上呼吸道分离得到,当时该病毒主要导致犬传染性喉气管炎,部分犬还出现喉炎、坏死性细支气管炎甚至肺炎的症状,但不会引发肝炎,该毒株被命名为A26株。研究发现,CAV-2与CAV-1在毒力、可溶性抗原识别结构、细胞侵染区域和血红蛋白凝集区域等方面存在相似性。因此,使用CAV-2进行免疫,可以有效保护犬免受CAV-1强毒引发的传染性肝炎。
八 实验犬微生物检测标准
CAV是哺乳动物腺病毒属中极具致病性的病毒之一,包括CAV-1和CAV-2。我国目前关于犬细小病毒感染的主要检测标准包括:《实验动物 犬腺病毒检测方法》、《犬腺病毒PCR检测方法》、《大熊猫检疫技术-犬腺病毒实验室检测技术规范-PCR方法》、《犬传染性肝炎诊断技术》、《犬传染性肝炎检疫技术规范》和《实验动物 传染性犬肝炎病毒检测方法》等,但是尚缺乏相关的生物学特性数据,对现有微生物标准中检测参数“查缺补漏”,及时更新标准体系,做到符合国情同时与国际接轨,是完善和提高我国实验动物微生物学质量控制体系急需开展的基础性工作。本课题采取政策研究、文献、比较研究及问卷调查、现场调研等方法,比较研究国内外农用实验动物的微生物监测项目要求、检测方法标准,对现有实验动物微生物监测标准进行“查漏补缺”,建立监测及检测标准。
参考文献:
[1] R.G. Green, N.R. Ziegler, B.B. Green, E.T. Dewey, EPIZOOTIC FOX ENCEPHALITIS. I. GENERAL DESCRIPTION, American Journal of Epidemiology (1) (1930) 1.
[2] J. Ditchfield, L.W. Macpherson, A.A. Zbitnew, Association of Canine Adenovirus (Toronto A 26/61) with an Outbreak of Laryngotracheitis ("Kennel Cough"): A Preliminary Report†, The Canadian veterinary journal. La revue veterinaire canadienne 3(8) (1962) 238-247.
[3] G.A. Fairchild, D. Cohen, Serologic study of a canine adenovirus (Toronto A26/61) infection in dogs, American Journal of Veterinary Research 30(6) (1969) 923.
[4] R.G. Marusyk, Comparison of the immunological properties of two canine adenoviruses, Canadian Journal of Microbiology 18(6) (1972) 817-823.
[5] R.G. Marusyk, E. Norrby, U. Lundqvist, Biophysical Comparison of Two Canine Adenoviruses, Journal of Virology 5(4) (1970) 507.
[6] L.J. Swango, G.A. Eddy, L.N. Binn, Serologic comparisons of infectious canine hepatitis and toronto A26-61 canine adenoviruses, American Journal of Veterinary Research 30(8) (1969) 1381.
[7] T. Yamamoto, R.G. Maruysk, Morphological Studies of a Canine Adenovirus, Journal of General Virology 2(1) (1968) 191-194.
[8] A.J. Davison, M. Benko, B. Harrach, Genetic content and evolution of adenoviruses, The Journal of General Virology: A Federation of European Miorobiological Societies Journal (11) (2003) 84.
[9] M.D. Morrison, D.E. Onions, L. Nicolson, Complete DNA sequence of canine adenovirus type 1, Journal of General Virology 78 ( Pt 4)(4) (1997) 873-878.
[10] 王东, 犬1型腺病毒强毒株的分离与鉴定及其对犬的实验感染初步研究, 长春理工大学, 2009.
[11] M. Appel, S.I. Bistner, M. Menegus, D.A. Albert, L.E. Carmichael, Pathogenicity of low-virulence strains of two canine adenovirus types, American Journal of Veterinary Research 34(4) (1973) 543-550.
[12] R.G. Marusyk, T. Yamamoto, Characterization of a canine adenovirus hemagglutinin, Canadian Journal of Microbiology 17(2) (1971) 151.
[13] 葛艳华, Asia-1型犬瘟热病毒分离株H蛋白免疫原性分析及重组犬腺病毒2型的构建, 东北农业大学 (2009).
[14] 闫喜军, 姜莉莉, 柴秀丽, 吴威, 丛丽, 邵西群, 王凤雪, 狐传染性脑炎活疫苗抗体消长规律的研究, 经济动物学报 (02) (2006) 70-72.
[15] 廖均乐, 犬腺病毒2型分离鉴定及感染模型建立与初步应用, 2022.
[16] 罗国良, 闫喜军, 钟伟, 狐狸传染性脑炎病原学研究进展, 动物医学进展 (08) (2008) 63-66.
[17] Caudell, A. W, Confer, R. W, Fulton, Berry, J. T, Saliki, G. M, Fent, Diagnosis of infectious canine hepatitis virus (CAV-1) infection in puppies with encephalopathy, Journal of veterinary diagnostic investigation : official publication of the American Association of Veterinary Laboratory Diagnosticians, Inc (2005).
[18] S.J. Hornsey, H. Philibert, D.L. Godson, E.C.R. Snead, Canine adenovirus type 1 causing neurological signs in a 5-week-old puppy, BMC Veterinary Research 15 (2019).
[19] 李. 喻昌盛, 中西医结合治疗犬的呼吸道综合征, 中国兽医杂志 (03) (2005) 54.
[20] 廖均乐, 孙春艳, 刘彩红, 崔宁宁, 刘玉秀, 田克恭, 张许科, 犬腺病毒研究进展, 中国兽医杂志 59(02) (2023) 90-92.
[21] A. Balboni, F. Dondi, C. Agnoli, R. Verin, M. Battilani, Novel sequence variants of viral hexon and fibre genes in two dogs with canine adenovirus type 1-associated disease, The Veterinary Journal 223 (2017) 73.
编辑信箱
欢迎您推荐或发布各类关于实验动物行业资讯、研究进展、前沿技术、学术热点、产品宣传与产业资源推广、产业分析内容以及相关评论、专题、采访、约稿等。
我要分享 >热点资讯
- 年
- 月
- 周





