猫杯状病毒感染与实验用猫质量控制
猫杯状病毒是由猫杯状病毒(Feline Calicivirus,FCV)感染引起的猫病毒性呼吸道传染病,主要表现为上呼吸道症状,即结膜炎、口腔炎、气管炎。FCV是单股的正链RNA病毒,无囊膜,发生抗原变异以及遗传突变的概率较大,属于杯状病毒科(Caliciviridae),水疱疹病毒属(Vesivirus),是一种能引起包括狮子、老虎以及猎豹等野生动物在内的所有猫科动物呼吸道疾病的病毒。由于隐形感染猫以及完全治愈猫都会继续排毒,有研究报道最长能达到75天,因此猫杯状病毒具有高度传染性且发病率高。FCV在猫科动物的健康方面仍是个复杂的课题,有必要通过持续的研究来加强对猫科动物遗传多样性的认识、改善疫苗功效和探索治疗新方案。
一、病原
分类地位:猫杯状病毒(FCV)分类上属于杯状病毒科(Caliciviridae),水疱疹病毒属(Vesivirus)。杯状病毒指一群有着同样典型外表的病毒。在小RNA病毒科的分类中,该科曾被归入一杯状病毒属。由于该属种间有明显区别而未被列入新分类学中。在1981年,由于该属的成员与大多数其他小RNA病毒有着明显的不同,国际病毒分类委员会决定将其划分为一个独立的科目。杯状病毒科目前包含四个不同的属,除了囊泡状病毒属之外,还进一步细分为免病毒属(Lagovirus)、诺瓦克病毒属(Norovirus)以及札幌病毒属(Sapovir us)。
1957年Fastier分离得到了猫杯状病毒,这是最早得到的一株FCV[1],在此之后在全世界各地都陆续分离到了毒株,甚至死亡的强毒株FCV-VSD被相继报道,强毒株感染的死亡率在50%~100[2],这曾经引发美国疫情的大面积爆发。近年来,FCV的研究在分子流行病学、临床诊断以及发病机制等方面均取得重大进展[3]。
形态学基本特征:杯状病毒指一群有着同样典型外表的病毒。衣壳是由32个中央凹陷、呈杯状结构的壳粒整齐排列而成的,这也是杯状病毒名称的由来。这些杯状的表面结构由90个壳粒以T=3二十面体对称形式组成。壳粒是病毒衣壳蛋白二聚体,分3个区域:上部分两叶结构、中央茎区、下部分壳状结构。衣壳的化学构成中仅包含一种分子量在73~76kDa范围内的多肽,由108个此类多肽组合而成[4]。在负染电子显微镜观察下,我们可以看到病毒粒子的表面呈现出典型的杯状结构,并且在电子显微镜下还能观察到少数病毒的空壳和无核部分。实心粒子的外表是白色的,空心粒子则缺少核酸且外表为白环状的结构[5]。
培养特性:猫杯状病毒不仅能在猫的肾脏、口腔、鼻腔、呼吸道上皮细胞以及胎肺原代细胞中进行大规模繁殖,还能在二倍体猫舌细胞系和胸腺细胞系中进行生长,通常在48小时内会出现显著的病理改变。受影响的细胞呈现圆缩状态,偶尔可以观察到葡萄粒状或团状的脱落现象。细胞核呈现圆形或椭圆形,其内仁消失,核外区域出现散在的凝结,同时伴有嗜酸性的白细胞入侵。猫杯状病毒有能力在源自海豚、犬、猴等多个动物种群的细胞内进行生长和壮大。由于其具有很强的致病性和传染性,并且对宿主有一定程度的依赖性,使得人们对于它也十分关注。这种病毒在细胞质中有着广泛的分布,其形态呈现为散乱或晶体排列,并且尚未形成包涵体。因此,至今我们还不能将这种病毒感染到像鸡胚这样的实验动物体内。猫杯状病是一种传染性极强的病毒性疾病,一旦感染就会导致大量死亡,并且具有高度致死率。在当前的临床实践中,这种疾病尚未有明确的治疗方法,因此主要是通过疫苗接种来进行预防。在Vero MA-104和MDCK细胞内,我们也发现了接种现象,经过5~6代的盲传,Vero和MA-104细胞中也出现了轻微的细胞变化[6],但这些变化是持续的,并且相对不稳定。
理化特性:猫杯状病毒病毒粒子在CsCI中浮密度为1.37~1.42g/cm。对脂溶剂(如乙醚、氯仿和脱氧胆酸盐)具有抵抗力;对pH的敏感性介于肠道病毒和鼻病毒之间,pH3时失去活力,pH4~5时稳定;50℃ 30min 灭活,MgSO,和MgCl,不能增强病毒对热的抵抗力,2% NaOH能有效灭活猫杯状病毒[7]。
猫杯状病毒是不具有血凝性的。血清学的研究结果显示,猫杯状病毒仅存在一个血清型。一些人持有观点,认为还有一种血清的变种存在。
基因组结构:FCV属于杯状病毒科Vesivirus属,是一种具有高度传播性的病原体。其在自然界中分布广泛,可引起多种疾病,主要感染人、犬及猫等哺乳动物。这个家族涵盖了一些知名的人类病原体,例如诺如病毒,还有一些特定于动物的病毒,例如兔出血病病毒和欧洲棕兔综合征病毒。杯状病毒家族的名字来源于颗粒上特有的杯状凹陷特征,它在自然界广泛分布于各种环境及宿主体内,但其感染主要发生在哺乳动物,尤其是猫、狗等小型猫科动物。FCV携带约7.5k碱基的单链RNA基因组,具有阳性意义,与其他宿主相关的基因也参与了其进化过程。在病毒复制过程中,缺少有效的校对机制有助于实现更高的突变率,从而促进其快速进化潜力[8]。病毒的基因组结构是非分段的,它由三个功能性的开放阅读框(ORF)组成,其在自然界中分布广泛,可引起多种疾病,主要感染人、犬及猫等哺乳动物。ORF1的主要功能是生成一种大型的多蛋白,然后进行切割以生成六种不同的非结构性蛋白,其中包括依赖于RNA的RNA聚合酶(RdRp),这在病毒的复制过程中起到了关键作用。这些蛋白是通过与核酸结合而发挥其功能,尽管结构蛋白是在基因组RNA中编码的,但它是由感染晚期的亚基因组RNA所产生的,这些蛋白质可以与宿主细胞膜上受体结合而发挥生物学作用。ORF2负责编码多种蛋白质,这些蛋白质在经过特定处理后,会释放出一种名为衣壳前导(LC)和主要衣壳蛋白(VP1)的微型蛋白质。它们可以与病毒表面受体结合并介导抗病毒过程。LC蛋白在Vesivirus属中显示出其独有的特性,并已被确定为在猫肾细胞培养液中产生能触发细胞病变效应的病毒所需的关键成分,由于它不存在于宿主体内或可从外界摄取,因此可以防止感染动物对它们进行免疫接种。这一独特性质让人们有能力通过将特定的蛋白质与其他已知的病毒抗原相结合,从而有效地控制病毒的感染过程并增强其免疫反应。VP1蛋白构成了病毒粒子外壳的核心部分,而ORF3主要负责编码VP2这一次级外壳蛋白。
二、流传病学
FCV主要对猫产生影响,除了野生的猫科动物,它们并没有特定的宿主或其他种类的宿主。对于人类来说,感染的风险相对较低。FCV样病毒有时会从狗的体内被分离出来,但它们在狗和猫的FCV流行病学研究中的具体作用仍然是一个未解之谜。FCV菌株TIG-1是在2014年成功地从西伯利亚虎的粪便样本中分离出来的。由于它不存在于宿主体内或可从外界摄取,因此可以防止感染动物对它们进行免疫接种。这种毒株有可能导致严重的肺炎,并有可能致命。本实验采用流式细胞仪检测了该株菌对多种常见致病菌和肿瘤相关病原微生物的增殖活性以及致病性变化情况。TIG-1菌株的生长趋势研究表明,在被感染后的12至36小时期间,与F9菌株相比,其病毒载量的增加速度更为迅猛。TIG-1 被确定为一种高毒力的 FCV 毒株,在受感染的猫中导致 100% 的发病率和致死率[9, 10]。
FCV的脱落主要是因为受到急性疾病困扰的猫的口腔和鼻腔中出现的分泌物,然而它们的血液、尿样和粪便也是这种现象的常见来源。猫在感染之后,可能在接下来的1至30天里还会脱落,其中少数会延续好几年甚至一生。尽管猫持续被暴露在外,但似乎有些猫对这种感染展现出了抵抗力,可能这源于免疫反应或者是遗传相关的原因。在遭受急性疾病感染的猫以及看起来已经完全康复但仍然是病毒携带者的猫,都有可能检测出 FCV。
病毒在生态环境中具有强大的持续生存本领,这主要是因为它能够在常温条件下的干旱表面生存几日甚至几周,即便是在较为寒冷和潮湿的环境下,其生存期还能显著延长。尽管母体源性抗体(MDA)或预先接种的疫苗可以缓解或消除临床症状,但这并不能预防感染。而且,接种疫苗或自然免疫的猫在亚临床感染后仍然可能成为携带者,这突显了沉默携带者在疾病流行病学中的重要性。这种特性使得人们能通过将该蛋白与其它已知的病毒抗原结合来控制这些病毒感染过程并提高其免疫原性。相较于更为稳定的多猫家庭,高周转率的收容所展示了更高的FCV遗传变异性,尽管这些基因发生突变会影响猫群的健康,但是它们不会导致猫群体间的相互传染,因为他们之间不需要进行隔离。猫舍、收容所和兽医诊所存在间接传播的问题,这种传播可能是通过污染物、人类、气溶胶或者跳蚤粪便来实现的。
一个特定的群体中高FCV发病率与高CFCV毒素的种类多样性有关联,这种关系可能源于少量持续感染的猫或猫种群中的其他成员再一次感染相同FCV病毒的变种或不同类型的毒株。猫群或其群体通常都可能会受到从不同家族演变出的各种病毒的感染。另外,单一猫上可能会感染多种FCV菌株,将新型微生物株导入到猫群和单个猫体内,可能会导致多种菌株受到感染,进一步触发基因重组和遗传多样性的增加;后者可能与猫在面对群体免疫反应时,选择抗原突变来规避反应有关,这可能进一步导致猫的群体内出现地域性感染。
三、临床症状
1.动物在被猫杯状病毒感染后,口腔中的溃疡成为其常见的标志性症状,有时它只是一个症状,并在鼻腔内可能发现相似的问题。被病态感染的猫精神状态显得低落,频繁地打喷嚏、嘴巴、鼻子和眼睛中分泌物明显增多,偶尔还会出现大量唾液分泌和角膜炎的症状。通常情况下,猫杯病毒的感染主要发生在口腔和呼吸道区域,虽然它具有很高的毒性,但也有可能扩散到肺部,可能引发肺水肿和间质性肺炎,表现为呼吸困难等临床症状。对该株菌进行了分离纯化和生物学特性测定。有时,我们也可能面临由呼吸道感染引发的致命症状,如隐性或严重的肺炎,这种情况在猫中是比较少见的,通常只影响到小猫。猫杯状病毒同样可能导致急性热性热病伴随多神经炎引发的跛行综合症,这一综合症在实验条件下可以被再次观察到。这揭示了跛行和口腔及呼吸道病症实际上是临床症状的两重极端,部分毒株倾向于表现一种,然而绝大部分毒株能够同时呈现两种临床表现症状。
2.到目前为止,在人类的临床症状上还没有关于猫杯形病毒感染的报道。
四、发病机制
FCV 与杯状病毒科的其他研究方向截然不同,一直是探索分子致病机制的宝贵工具,尤其是它在细胞培养环境下的培育能力所带来的好处。此项研究在深化我们对病毒致病机制和消毒方法的理解上起到了关键作用,如果没有及时采取适当的治疗措施,则有可能发展成为慢性支气管炎或者肺间质纤维化,最终出现呼吸衰竭而死亡。在猫的体内,FCV的感染主要集中在口部和咽喉部位,这会导致短暂的病毒性血症,并进一步将FCV传播到各种通过免疫组化测试和电子显微镜观察,确认VSFCV感染了猫的上皮和内皮细胞,从而引发细胞死亡、对血管造成损害以及高死亡风险。VS-FCV菌株主要针对fJAM-A,这是上皮细胞与内皮细胞连接位置上发现的一种受体,这可能会引起连接区域的损害和泄露。此外,猫体的血小板与血白细胞上发现了fJAM-A受体,这表明FCV呈现出血流分布模式,这一点在血液中FCV RNA的检测结果上也得到了体现。已发现将 fJAM-A 表达系统引入非允许细胞可将其转化为 FCV 的允许细胞,突出了 fJAM-A 蛋白的重要受体作用[11]。
除了明显的口腔相关症状之外,FCV同样能够引发跛行现象,这一现象被普遍称为跛行综合症。跛行综合症与免疫复合物紧密相关,而FCV可以在受其影响的关节中得到检测,以跛行和发烧为特征的多发性关节炎可发生在 FCV 感染或接种疫苗后的猫身上,并被假设为 III 型超敏反应[12]。在这种反应中,抗原-抗体复合物形成并在关节中积累,引发急性炎症反应。虽然这种综合征与FCV有直接关联,但在FCV野应变所导致的复合感染症或某些例外状况下,疫苗菌的再次激活通常被视为主导的触发元素。感染了的猫显示了细胞因子水平的上升,特别是IL-10、TNF-α 以及MIP-1alpha,这指示着全身范围内的炎症反应。
在细胞培养过程中,FCV的感染会导致细胞形状变圆和膜起泡,产生特定的细胞病理变化。从分子学的角度,研究揭示在细胞培育过程中,FCV的感染会触发线粒体途径的活化,进一步导致半胱天冬酶的活性增强和细胞走向凋亡。FCV为了规避宿主的保护,FCV 采用了各种策略,包括抗原漂移和转移。FCV 容易出错的 RNA 聚合酶导致突变的持续积累(抗原漂移),并且还记录了不同 FCV 菌株之间的重组事件(抗原转移),这些变化可导致病毒表位发生重大改变[8],这可能会通过中和抗体来降低识别能力,或增强 FCV 与细胞受体结合的能力,从而增加其传染性。FCV 使用的另一种免疫逃避策略涉及抑制宿主蛋白质合成,这一过程称为宿主“关闭”,这种机制将宿主的蛋白质合成限制在病毒复制所需的必需蛋白质上,从而损害了宿主的抗病毒能力。
五、诊断
多种病原原因都可能导致猫的气道问题,且其症状有很多相似之处,所以准确的诊断会面临一定的障碍,这需要依赖实验室的综合检查来进行。
1.在进行病毒的分离与识别方面,在该病的急性期内,可以从眼结膜、鼻腔分泌物以及咽喉部和溃疡区的组织中取出样本,并利用猫源细胞来进行有效的病原分离工作。尽管我们可以在血液样本中检测到病毒的存在,但是利用血液中的物质进行组织培养是不推荐的,可以考虑将这些病料植入猫的肾脏细胞系中。猫是人类最常见的宠物之一,也是许多疾病的易感动物,在没有发现任何疾病的情况下,接种后的3至5天内,我们会启动细胞传代的试验。若连续传六代但未见任何病症,则将其定义为阴性。面对出现(F81)细胞的情况,在吸附1小时之后,替换为细胞的维持液,进行3至5天的培养。然后每天都要检测是否有细胞发生了病变(细胞圆缩、脱顺时针逆时针病变的细胞),并在冻融3次后,在-20℃的环境中进行保存,接着利用PCR等技术进一步检测病毒的存在。
2.为了评估猫杯中状病毒的相关抗体,血清学试验的中和试验被视为主要的参考方式,尽管这种方法在时间和操作上都非常复杂,对于大型样本的检验并不合适。此种方法首先对血清进行稀释并在37℃下感觉与200TCID病毒反应一小时,然后接种F81细胞,仔细检查细胞的病变情况,旨在获取猫杯状病毒的中和抗体效价。
3.根据组织病理学的诊断,病猫会出现舌部和腭部的水泡破损和溃疡,而且这些溃疡区域的边缘和基底区域会有大量嗜中性白细胞的浸润现象。在肺部,我们发现了纤维素性肺炎(这只是病猫在下呼吸道的症状)和间质性肺炎;这种肺炎在肺泡中可观察到蛋白性渗出和巨噬细胞的积聚,同时,肺泡及其之间的空隙也被单核细胞所浸润。在支气管和细支气管的结构中,常常可以观察到大量的蛋白质渗出、单核细胞和脱落的上皮细胞,这种方法也可用于其它一些组织器官或肿瘤细胞,其大脑和小脑的石蜡切片也可见中等程度的局灶性神经胶质细胞增生及血管周围套出现。
4.在分子生物学的领域中,得益于分子生物学的持续进步和猫杯状病毒的基因组序列测定技术,RT-PCR已逐渐被广泛用于检测猫杯状病毒。这种方法对于检测猫杯状病毒的敏感度极高,因此已经是目前检测猫杯状病毒的主流技术。
检测标准:
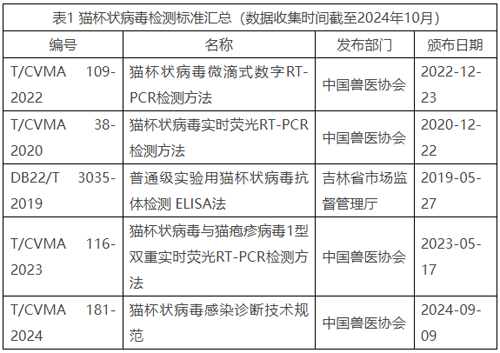
表1 猫杯状病毒检测标准汇总(数据收集时间截至2024年10月)
六、防治措施
FCV的特点是缺少磷脂的双层包膜,因此展现出了很高的韧性。RT-qPCR技术能在脱落停止后的28天内,在感染猫的环境中检测到FCV RNA的存在,尽管在任何时候都没有检测到具有复制能力的病毒[13]。在动物医院和收容所,不断接收免疫、疫苗和疾病背景未知的新猫,再加上FCV的长期环境稳定性,这构成了一个巨大的风险。因此,保持卫生和进行消毒是非常关键的,这包括确保所有表面都被彻底清洁,并采用已知对FCV有效的消毒剂,例如次氯酸钠(2,700 ppm,1 分钟)、加速过氧化氢(35,000 ppm,10 分钟)、醛 (2%) 或过氧一硫酸钾(1%,10 分钟)[14]。考虑到这两种病原体在病毒属性上的相似性,针对人类诺如病毒的高效杀病毒消毒剂同样适用于FCV。针对由FCV导致的URTD猫,治疗策略主要集中在支持性的护理措施上,这包括进行静脉输液、使用非甾体抗炎药、实施雾化疗法,以及提供口感极佳的食物以维持其营养状态。
重组猫干扰素 omega (feIFN-ω) 已经展现出降低临床症状和FCV复制的能力。尽管现在的市场上并没有直接针对FCV的抗病毒药物,但相关研究已经探讨了可能的治疗方法。feIFN-ω 和甲氟喹的组合在抑制 FCV 复制方面显示出前景。硝唑尼特和咪唑立滨在体外和体内均显示出抗病毒活性,表明具有潜在的治疗益处[15]。药物筛选已确定处理是通过在体外抑制 HSP70 表达作为 FCV 感染的抑制剂。实验环境中已经证明了几种抗病毒药物,例如利巴韦林、多聚4-苯乙烯磺酸钠、甲氟喹和其他一些天然化合物,对FCV复制具有显著的抑制作用,虽然这样,但它们在人体内的治疗效果还不是很明确。血清中含有FCV、猫疱疹病毒(FHV)和猫细小病毒(FPV)的抗体,这在治疗急性病毒性猫URTD方面展示了显著的治疗效果。
针对 FCV 感染所导致的猫慢性牙龈口炎 (FCGS) 的治疗方法,研究者们已经尝试了各种途径,这其中涵盖了牙齿的清洁、应用皮质类固醇疗法以及间充质干细胞疗法。当存在继发性细菌感染时,为 FCGS 开具广谱抗生素[16]。泼尼松龙和 felFN-ω 被认为用于管理 FCGS,此外,减轻压力、丰富环境和保持良好的卫生对于预防多猫家庭的 FCGS 至关重要。
疫苗注射是预防FCV感染的关键环节,它能够避免严重的临床表现、炎症反应并降低病毒的脱落风险。无论是改良的活疫苗还是灭活疫苗,在市场上都是可以购买的。新兴的疫苗技术,例如mRNA疫苗和亚单位疫苗,具有广阔的发展前景,但目前还没有实现商业化。疫苗接种指导方针综合考虑了年龄、健康状态、生活习惯以及居住环境等多个变量,以便确定最合适的疫苗接种时间和种类。
FCV的脱落和相关的临床表现都与抗FCV IgM抗体的急剧增加有关。IgM水平最初的上升速度很快就被IgG抗体的迅速增长所替代,这一变化与病毒的中和活性初始阶段是一致的。这项研究证明,IgG抗体在中和过程中起到了核心作用,而在中和反应的初始阶段,IgM抗体显得尤为关键,然而,区分疫苗诱导的抗体和野生型抗体具有挑战性。此外,研究调查了唾液和血清中 IgA 抗体的存在,观察到唾液中 IgA 抗体的峰值水平比在血清中更早检测到,这表明唾液 IgA 在早期防御 FCV 中具有潜在作用[17]。
按照传统的疫苗接种方案,建议在8-9周龄和12周龄时进行第一次接种,随后每年进行加强剂的接种,关于这个时间表是否有效,一直是一个备受争议的议题。有证据显示,由于MDA的持续存在,并不是所有的小猫在12周前都能建立起充分的免疫系统,虽然目前对免疫程序的优化已进行了大量研究,但仍没有明确结果。免疫系统的持续时长可能存在差异,特别是在面对来自不同来源的攻击时,目前正在研制新型疫苗,以应对免疫应答过程中出现的变化。FCV毒株间抗原的多样性可能会偶尔导致疫苗失效,因此,疫苗改进的方向包括增强交叉反应性、减少攻击病毒的脱落和预防持续感染。这些努力可以通过使用不同类型的候选疫苗来实现,但它们也面临着挑战,并且由于缺少保护性的生物标记物,激发实验在评定疫苗效果上变得尤为关键。
FCV疫苗通常是与FHV或FPV疫苗一同使用的,含有佐剂成分的灭活疫苗有可能引发注射部位的肉瘤风险。因此,目前正在研究一种新的疫苗形式以降低这种潜在风险,不过一款专为FCV设计的非佐剂灭活疫苗(由两种灭活病毒株组合制成)已经在欧洲和日本市场上推出。这种疫苗可通过将免疫原从感染动物中去除而减少潜在致癌危险,采用改进后的活性疫苗也是一个需要考虑的因素,因为这些疫苗有可能引发FCV毒株的扩散,进而可能导致免疫逃避变体的产生。通过将重组抗原用免疫原性较好的单克隆抗体制备成混合抗原来评价这些疫苗,抗体的检测在预测保护效果上的重要性是受限的,因为它可能与真实的户外曝露不太相关。研究发现了一个用于评估疫苗效果的有效方法,建议为已经康复的健康猫接种疫苗,考虑到 MDA 和风险因素,小猫和老年猫的疫苗接种策略有所不同。对最佳再接种间隔进行了辩论,建议范围从低风险情况下的三年加强剂到高风险环境中的年度加强剂[8]。
七、实验用猫微生物检测标准
猫杯状病毒是一种能导致包括狮子、老虎和猎豹在内的所有猫科动物出现呼吸道问题的病毒,其主要症状包括结膜炎、口腔炎和气管炎。在自然条件下,这种病主要发生于幼龄猫,鉴于隐形感染的猫和完全治愈的猫都会持续进行排毒过程,这也意味着猫杯状病毒具有很高的传播性。我国目前关于猫杯状病毒感染的主要检测标准包括:《猫杯状病毒感染诊断技术规范》、《猫杯状病毒与猫疱疹病毒1型双重实时荧光RT-PCR检测方法》、《普通级实验用猫杯状病毒抗体检测 ELISA法》、《猫杯状病毒实时荧光RT-PCR检测方法》和《猫杯状病毒微滴式数字RT-PCR检测方法》等,尽管我们还没有相关的生物学特性数据,但本研究通过政策研究、文献分析、比较研究、问卷调查和现场调查等多种方法,对国内实验动物的微生物监测项目要求和检测方法标准进行了比较研究,目的是对现有的实验动物微生物监测标准进行“查漏补缺”,并建立相应的监测和检测标准。
参考文献:
[1] FASTIER L B. A new feline virus isolated in tissue culture [J]. American journal of veterinary research, 1957, 18(67): 382-9.
[2] 杨旭. 猫细小病毒、猫杯状病毒的分离鉴定及遗传进化分析 [D], 2022.
[3] 燕超. 广西和新疆地区蝙蝠病毒组及小型环状DNA病毒遗传多样性研究 [D], 2019.
[4] ALVAREZ A L, PARRA F. Truncated Precursor of Feline calicivirus Major Capsid Protein: A Product Relevant for Replication, or an Aberrant Translation Artifact? [J]. Intervirology, 2021, 64(2): 108-10.
[5] CUBILLOS-ZAPATA C, ANGULO I, ALMANZA H, et al. Precise location of linear epitopes on the capsid surface of feline calicivirus recognized by neutralizing and non-neutralizing monoclonal antibodies [J]. Veterinary Research, 2020, 51(1).
[6] PHONGROOP K, RATTANASRISOMPORN J, TANGTRONGSUP S, et al. High-resolution melting analysis for simultaneous detection and discrimination between wild-type and vaccine strains of feline calicivirus [J]. Veterinary Quarterly, 2023, 43(1): 18-.
[7] QU Z, KANG H, CUI C, et al. Purification-induced damage to calicivirus particles at near-atomic resolution [J]. Journal of General Virology, 2022, 103(5).
[8] HOFMANN-LEHMANN R, HOSIE M J, HARTMANN K, et al. Calicivirus Infection in Cats [J]. Viruses, 2022, 14(5).
[9] TIAN J, KANG H, HUANG J, et al. Feline calicivirus strain 2280 p30 antagonizes type I interferon-mediated antiviral innate immunity through directly degrading IFNAR1 mRNA [J]. PLoS Pathog, 2020, 16(10): e1008944.
[10] TIAN J, LIU D, LIU Y, et al. Molecular characterization of a feline calicivirus isolated from tiger and its pathogenesis in cats [J]. Vet Microbiol, 2016, 192: 110-7.
[11] FUMIAN T M, TUIPULOTU D E, NETZLER N E, et al. Potential Therapeutic Agents for Feline Calicivirus Infection [J]. Viruses, 2018, 10(8).
[12] HARTMANN K, EGBERINK H, MöSTL K, et al. Feline Injection-Site Sarcoma and Other Adverse Reactions to Vaccination in Cats [J]. Viruses, 2023, 15(8).
[13] CONLEY M J, MCELWEE M, AZMI L, et al. Calicivirus VP2 forms a portal-like assembly following receptor engagement [J]. Nature, 2019, 565(7739): 377-81.
[14] CHIU S, SKURA B, PETRIC M, et al. Efficacy of common disinfectant/cleaning agents in inactivating murine norovirus and feline calicivirus as surrogate viruses for human norovirus [J]. Am J Infect Control, 2015, 43(11): 1208-12.
[15] CUI Z, LI D, XIE Y, et al. Nitazoxanide protects cats from feline calicivirus infection and acts synergistically with mizoribine in vitro [J]. Antiviral Res, 2020, 182: 104827.
[16] FONTES A C, VIEIRA M C, OLIVEIRA M, et al. Feline calicivirus and natural killer cells: A study of its relationship in chronic gingivostomatitis [J]. Vet World, 2023, 16(8): 1708-13.
[17] SPIRI A M. An Update on Feline Calicivirus [J]. Schweiz Arch Tierheilkd, 2022, 164(3): 225-41.
编辑信箱
欢迎您推荐或发布各类关于实验动物行业资讯、研究进展、前沿技术、学术热点、产品宣传与产业资源推广、产业分析内容以及相关评论、专题、采访、约稿等。
我要分享 >热点资讯
- 年
- 月
- 周





