张建团队利用小分子诱导信号,首次从小鼠桑葚胚中捕获新型多潜能滋养外层干细胞系MTSC
在哺乳动物胚胎发育的起始阶段,第一次关键的细胞命运抉择发生在桑椹胚(Morula)时期,将胚胎细胞分化为滋养外胚层(Trophectoderm, TE)和内细胞团(Inner Cell Mass, ICM)。因此,滋养外胚层干细胞是研究胚胎植入和胎盘分化的重要模型。然而,其信号调控和发育分化过程仍有许多未知。目前,有限的滋养外胚层干细胞系具有较强的异质性,对应的发育时期较晚(E4.5-6.5,围着床期),且发育潜能尚存在不足。因此,获得更早期的具有更高发育潜能的滋养层干细胞,是完善类囊胚(Blastoids)构建体系,实现类囊胚高效植入子宫的关键途径之一。
2025年8月14日,云南大学张建教授(现已任职复旦大学生命科学学院)团队在Nature Cell Biology杂志上发表了题为"Mouse trophectoderm stem cells generated with morula signalling inducers capture an early trophectoderm state"的研究论文。该研究首次成功建立并系统表征了来源于小鼠32细胞桑椹胚(E3.0)的新型滋养外胚层干细胞系——Morula-derived Trophectoderm Stem Cell (MTSC)。这项工作填补了滋养层发育研究模型在发育时间线上的空白,并揭示了早期滋养外胚层的独特分子特征和信号调控,为理解胚胎植入前发育分化提供了新的研究模型。

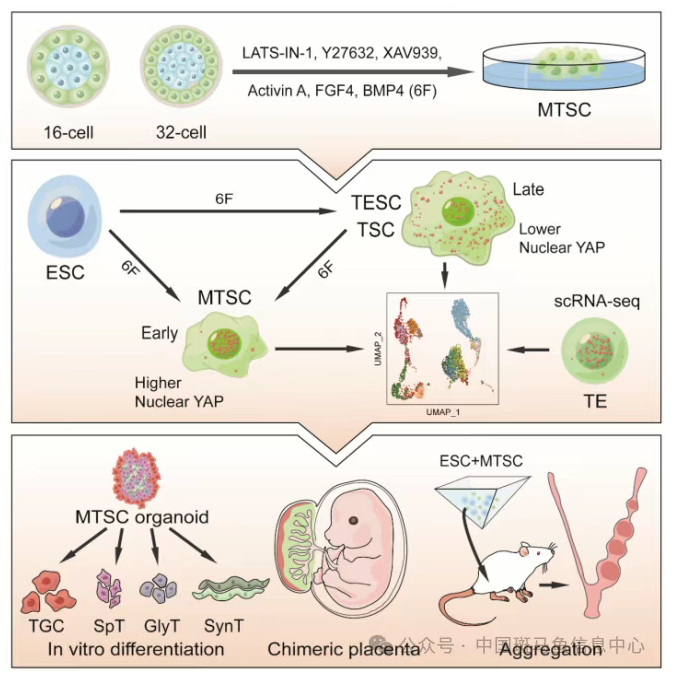
研究人员设计了一种模拟桑椹胚阶段关键信号通路的培养基组合(包含Hippo通路抑制剂LATS-IN-1、Rho激酶抑制剂Y27632、Wnt通路抑制剂XAV939、FGF4、BMP4和Activin),成功从32细胞期小鼠胚胎的外部细胞(代表最早的TE谱系)中高效衍生出MTSC单细胞转录组测序(scRNA-seq)分析显示,MTSC的分子特征与体内E3.0-3.5胚胎的滋养外胚层细胞高度相似,而与代表晚期滋养外胚层状态的经典TSC (E5.5-6.5) 和TESC (E4.5-5.5) 显著不同。MTSC表现出独特的形态学特征(细胞更小、更紧密、更立体),并维持YAP1蛋白的核定位(这是早期TE的关键标志),在体外可稳定传代超过30代而不发生自发分化。
分化潜能方面,将MTSC注射到宿主桑椹胚或囊胚中,MTSC能有效整合到囊胚的滋养外胚层。移植后,MTSC特异性地整合到胎盘组织中,并分化为胎盘滋养层各种终末细胞类型;同时,MTSC能在3D培养条件下高效形成滋养层类器官(Trophoblast Organoids)。这些类器官具有清晰的管腔结构,去除维持因子后能迅速分化为表达多种胎盘特异性标记物(如EPCAM, CD71, TPBPA, SYNA)的细胞群体。单细胞也测序证实,分化后的类器官包含多种与体内胎盘滋养层细胞相似的亚群(如S-TGC-like, SpT-like, SynT-like细胞等)。
重要的是MTSC诱导体系具有强大的“重编程”能力:可以将胚胎干细胞(ESC)重编程为MTSC样细胞(MTSC-like cells)。功能上,这些ESCs重编程来源的MTSC样细胞注射到囊胚后,其子代细胞能特异性地整合到胎盘组织中并分化为多种滋养层细胞。这一发现表明ICM与TE谱系在非基因编辑的前提下不可逆分离的观念,表明强烈的滋养外胚层信号环境可以逆转多能性状态,将ESC推向滋养外胚层命运。此外,研究者发现,将短暂分化后的MTSC(称为MITE细胞)与ESC聚集,形成的Blastoids(MITE-Blastoids)表现出更清晰的囊胚腔和极性(类似体内囊胚的Polar-Mural轴)。
综上,这项由张建教授团队完成的研究,是滋养外胚层领域的一项重要成果。MTSC的建立及相关发现,为我们深入理解哺乳动物胚胎细胞命运决定、滋养外胚层谱系的建立与分化提供了新的理论依据。同时,研究所使用的分子信号组合不仅具有强大的TE谱系重编程能力,其核心思路(模拟特定发育阶段的信号环境)可能为在其它物种(包括人类)中建立类似早期滋养层干细胞模型提供借鉴。
云南大学博士生高亚可(现成都双楠医院生殖中心实验室负责人)和李明颖(现云南省第一人民医院生殖医学科)为论文的共同第一作者。云南大学/复旦大学生命科学学院张建教授为论文通讯作者。论文研究得到了广州国家实验室Jose Silva 教授团队,包括关炜、李欢欢博士的大力支持。
编辑信箱
欢迎您推荐或发布各类关于实验动物行业资讯、研究进展、前沿技术、学术热点、产品宣传与产业资源推广、产业分析内容以及相关评论、专题、采访、约稿等。
我要分享 >热点资讯
- 年
- 月
- 周





