上海海洋大学吕为群团队发现foxo1a在维持中枢神经系统抗氧化稳态中的关键作用
髓鞘是一种包裹神经元轴突的密集多层膜状结构,通过加速神经网络信号整合以及提高神经信号传递的效率和精度来实现快速反应和增强感知能力,使脊椎动物能够发展出更复杂的行为模式和生理功能。重要的是,髓鞘能够提高信号传输速度,而无需增加轴突直径,从而适应复杂神经系统进化所需的大量轴突。从能量代谢的角度来看,有颌脊椎动物通常比无颌脊椎动物具有更高的代谢率,并且拥有更复杂的神经系统。在标准生理条件下,神经元主要通过线粒体氧化磷酸化来生成三磷酸腺苷ATP。然而,这一过程与线粒体呼吸链内电子泄漏所产生的活性氧(ROS)有关,导致有颌脊椎动物体内活性氧的积累量比无颌脊椎动物更多。值得注意的是,有颌脊椎动物似乎拥有有效的机制来降低活性氧过度积累以及由此产生的氧化损伤的风险。尽管如此,在有颌脊椎动物的进化生物学中,髓鞘和神经元在高效信号传导过程中如何抵御氧化损伤的具体机制仍是一个重大谜团。
近日,上海海洋大学吕为群团队在Redox Biology在线发表了题为“Guardian of Myelin and Neural Integrity: foxo1a through slc7a11 mitigating oxidative damage in myelin”的研究论文,该研究阐明了foxo1a在维持中枢神经系统抗氧化稳态中的关键作用,并为有颌脊椎动物中枢神经系统的适应性进化提供了新的见解。

本研究通过比较无颌与有颌脊椎动物的分化时间和基因家族异质性,确定了关键的FoxO基因家族成员foxo1a是有颌脊椎动物进化所必需的。发现foxo1a定位于斑马鱼的少突胶质细胞和髓鞘,在抗氧化保护中发挥关键作用。具体而言,发现敲除foxo1a基因会导致斑马鱼中枢神经系统髓鞘发育异常,少突胶质细胞、星形胶质细胞以及髓鞘标志物减少,并诱发“冻结”行为。进一步研究表明,这与foxo1a基因缺失后斑马鱼中枢神经系统的氧化应激反应和铁死亡有关。在机制上,发现foxo1a通过直接调控slc7a11基因的启动子活性,参与调节中枢神经系统的氧化应激反应和铁稳态。在应用方面,发现外源补充foxo1a能够在硫酸铜诱导的髓鞘损伤模型中发挥抗氧化保护作用。更重要的是,该研究发现foxo1a-slc7a11轴在斑马鱼和人类细胞中均存在相似性,提示foxo1a-slc7a11轴可能是一种进化上保守的有颌脊椎动物神经防御策略。
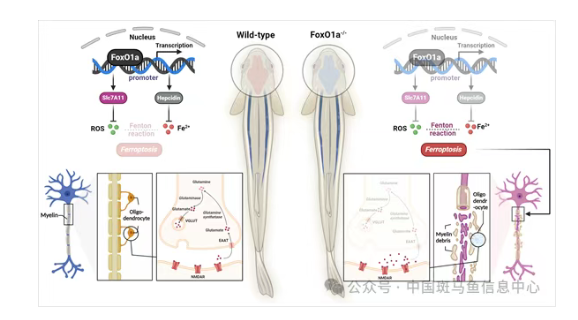
总之,本研究阐明了转录因子foxo1a在通过直接调控slc7a11的转录以减轻髓鞘氧化损伤方面所起的关键保护作用。有颌脊椎动物髓鞘的出现对于复杂神经系统的进化具有重要意义,但维持它的正常功能还需要增强这些动物的抗氧化应激机制。foxo1a在这些动物中的扩增为其快速的适应性进化与环境适应提供了坚实的遗传基础。将foxo1a基因整合进有颌脊椎动物基因组中的关键的遗传事件驱动了髓鞘的进化,从而让神经系统实现了升级。这些发现不仅增进了我们对无颌和有颌脊椎动物适应性进化之间差异与联系的理解,也为探究神经防御机制的进化特征提供了重要的数据与理论支持。国家水生生物种质资源库国家斑马鱼资源中心保藏有foxo1a的两个突变系(CZ1342, CZ1343)并对外提供。
上海海洋大学吕为群教授为该论文通讯作者。实验室博士生赵寅捷和李子康为该论文的共同第一作者。
编辑信箱
欢迎您推荐或发布各类关于实验动物行业资讯、研究进展、前沿技术、学术热点、产品宣传与产业资源推广、产业分析内容以及相关评论、专题、采访、约稿等。
我要分享 >热点资讯
- 年
- 月
- 周





